Inhalt
1. Einleitung
2. Aktuelle Situation und neue Bedrohungen
3. Lebenslange Bekämpfung wichtiger Wurm-Arten
4. Strategische Bekämpfung von Wurmbefall
4.1. Entwurmung von Hunden
4.2. Entwurmung von Katzen
5. Biologie, Diagnose und Bekämpfung von Würmern
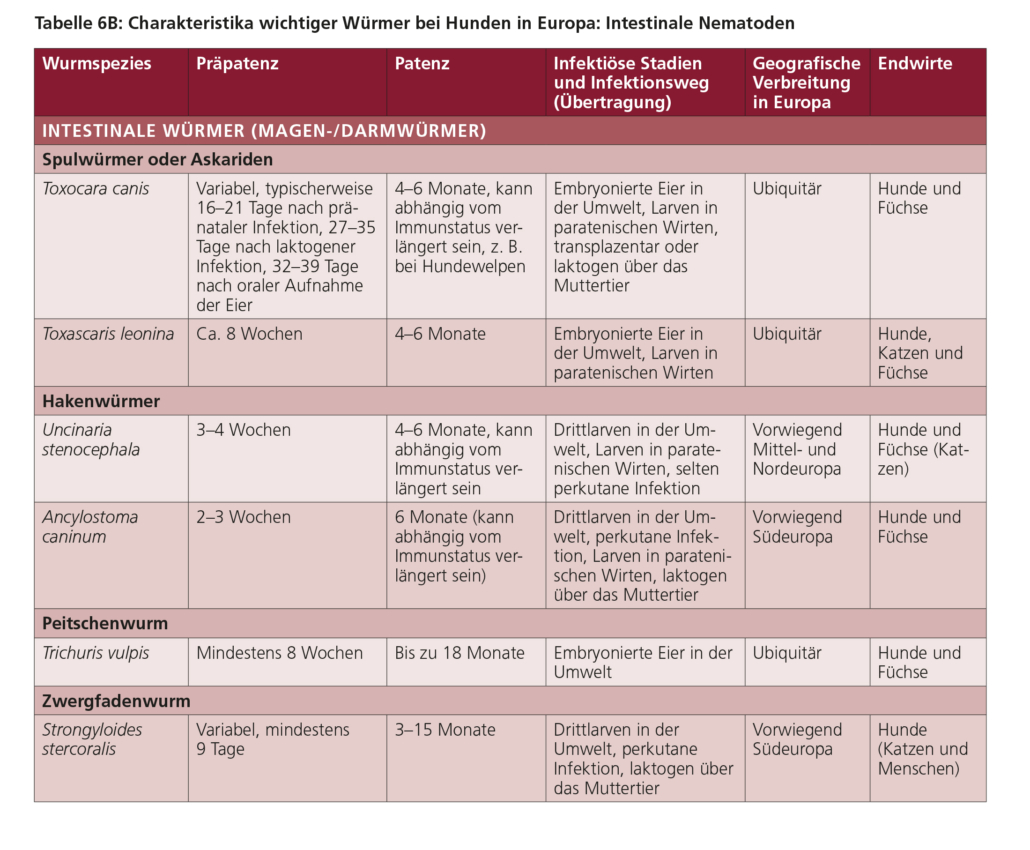
5.1. Spulwürmer (Toxocara spp., Toxascaris leonina)
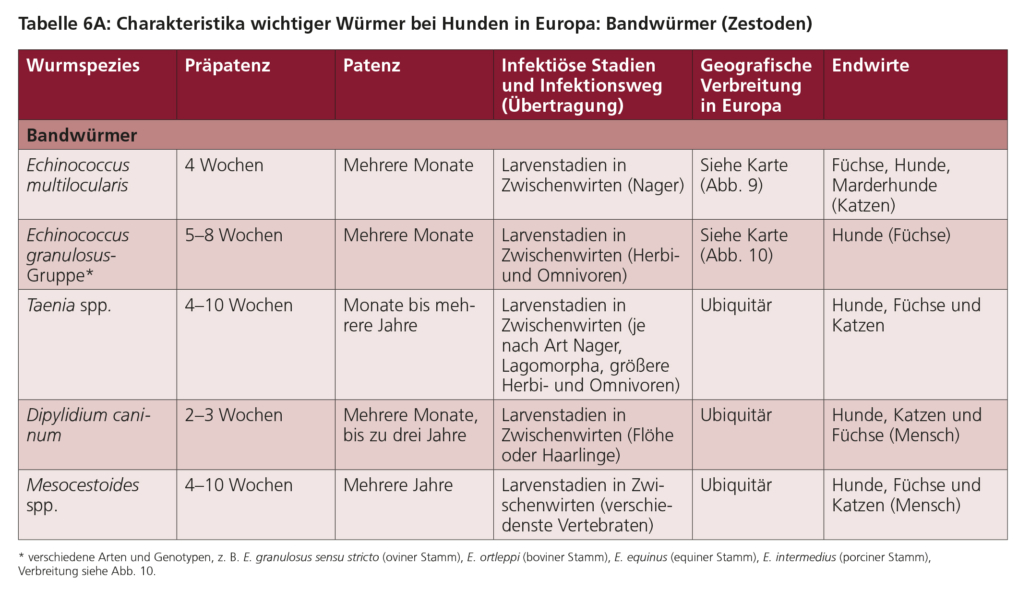
5.2. Bandwürmer
5.2.a. Echinococcus spp.
5.2.b. Dipylidium caninum
5.2.c. Taenia spp. und Hydatigera taeniaeformis
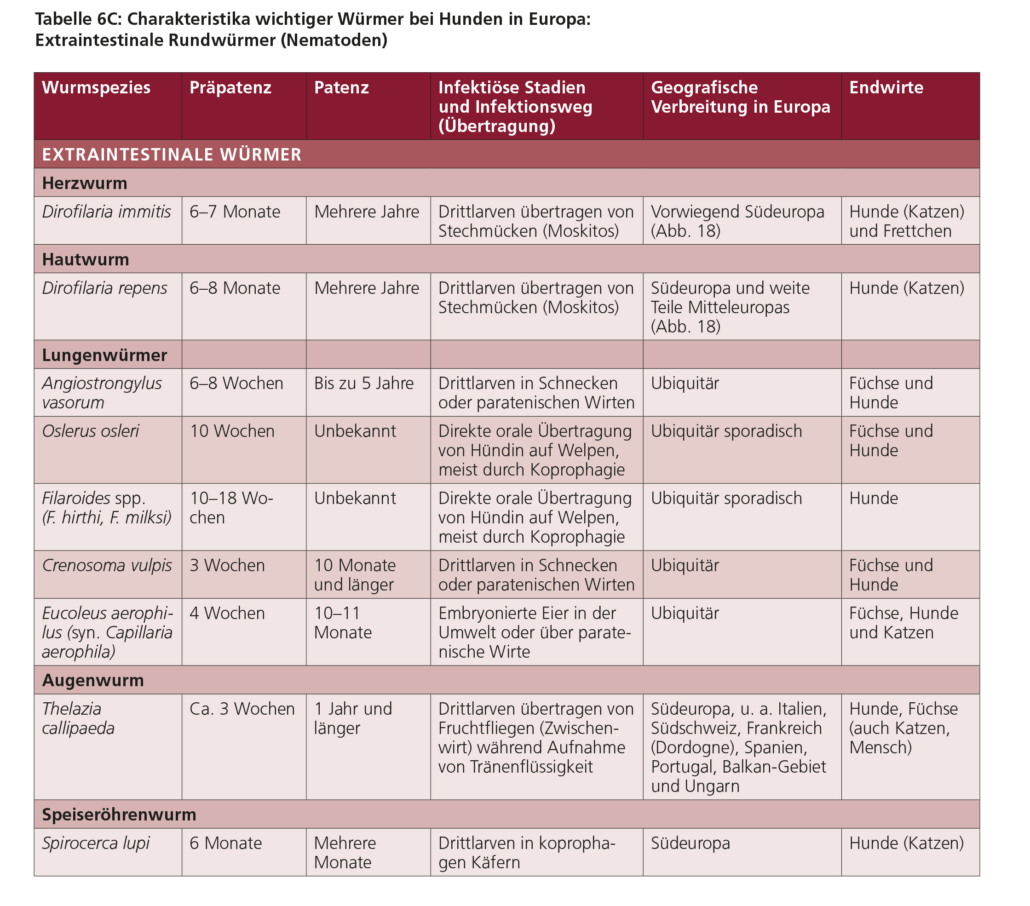
5.3. Herzwurm (Dirofilaria immitis)* und Hautwurm (Dirofilaria repens)
5.4. Lungenwürmer (Angiostrongylus vasorum, Crenosoma vulpis, Aelurostrongylus abstrusus)
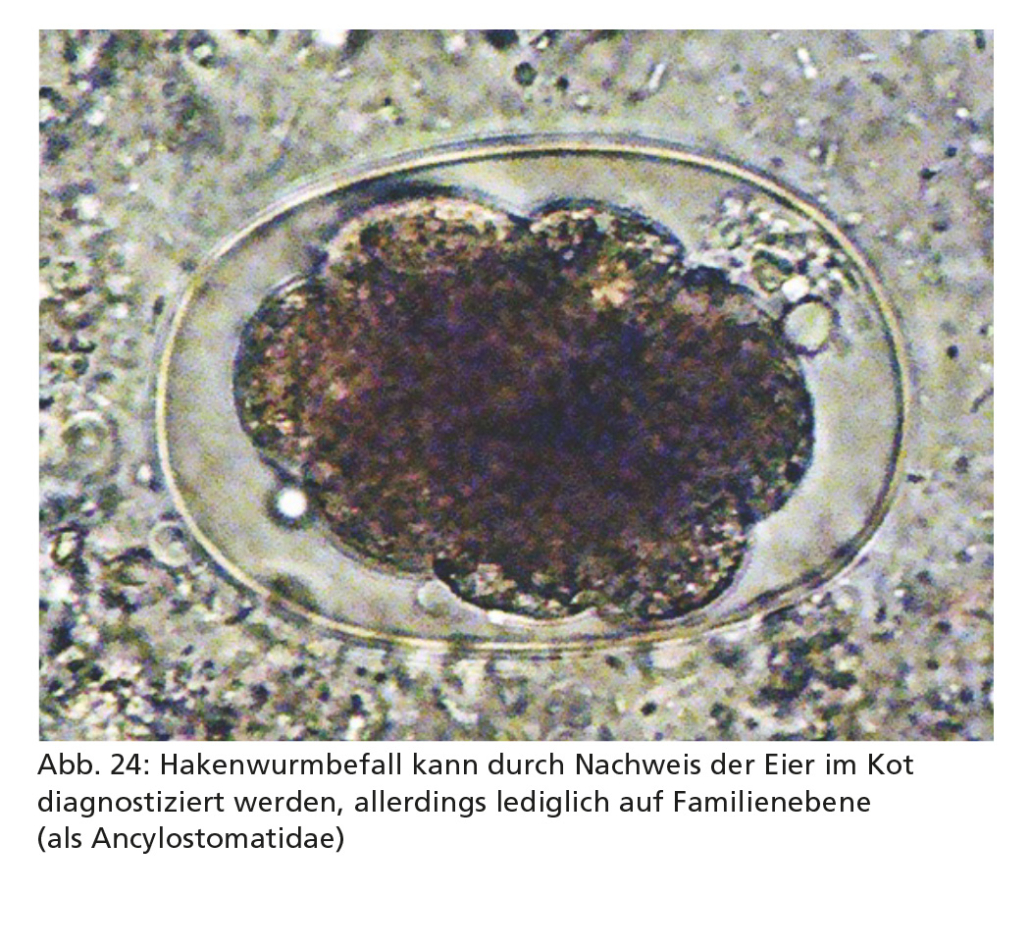
5.5. Hakenwürmer
5.6. Peitschenwürmer (Trichuris vulpis)
5.7. Zwergfadenwürmer (Strongyloides stercoralis)
6. Diagnose von Wurminfektionen
7. Individuelle Faktoren: Alter, Nutzung, Haltung, Ernährung und Reisen
8. Resistenzen gegen Anthelminthika und Bekämpfung von Parasitenstadien in der Umwelt
9. Prävention zoonotischer Parasitosen
10. Schulung von Praxisteams, TierbesitzerInnen und der Öffentlichkeit
1. Einleitung
In Europa können Hunde und Katzen mit einer Vielzahl verschiedener Helminthen (Nematoden, Cestoden und Trematoden) infiziert werden. Die wichtigsten Spezies nach Lokalisation im Wirt sind:
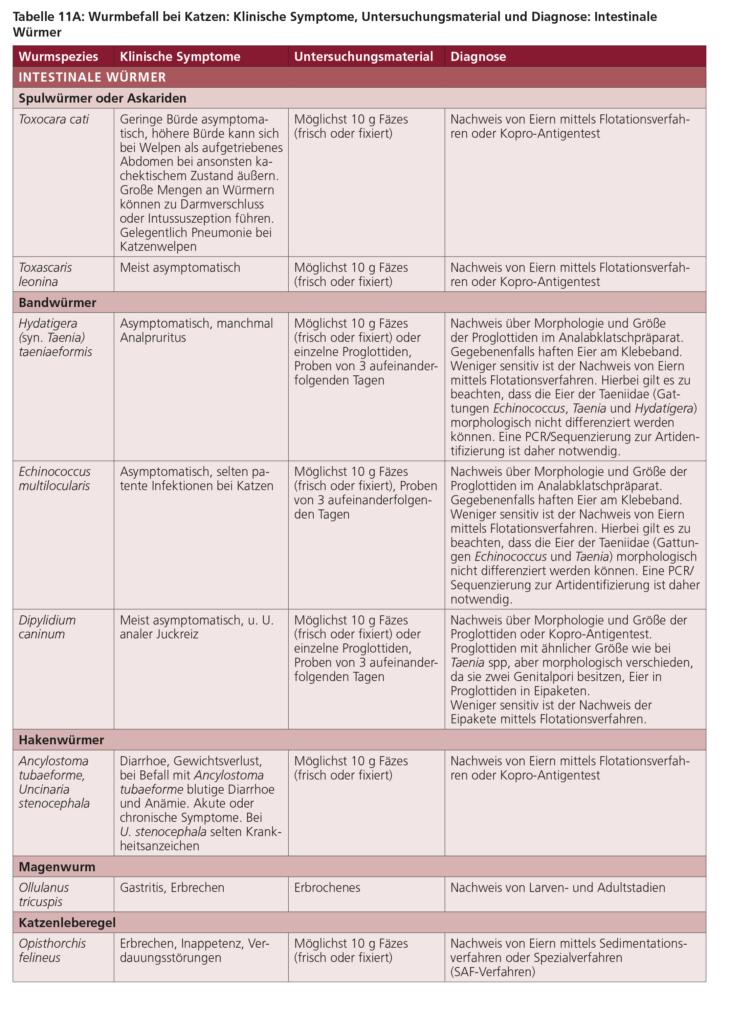
Intestinale Würmer:
- Spulwürmer (Toxocara und Toxascaris spp.)
- Bandwürmer (Echinococcus, Taenia und Dipylidium spp.)
- Hakenwürmer (Ancylostoma und Uncinaria spp.)
- Peitschenwurm (Trichuris vulpis)
- Zwergfadenwurm (Strongyloides stercoralis)
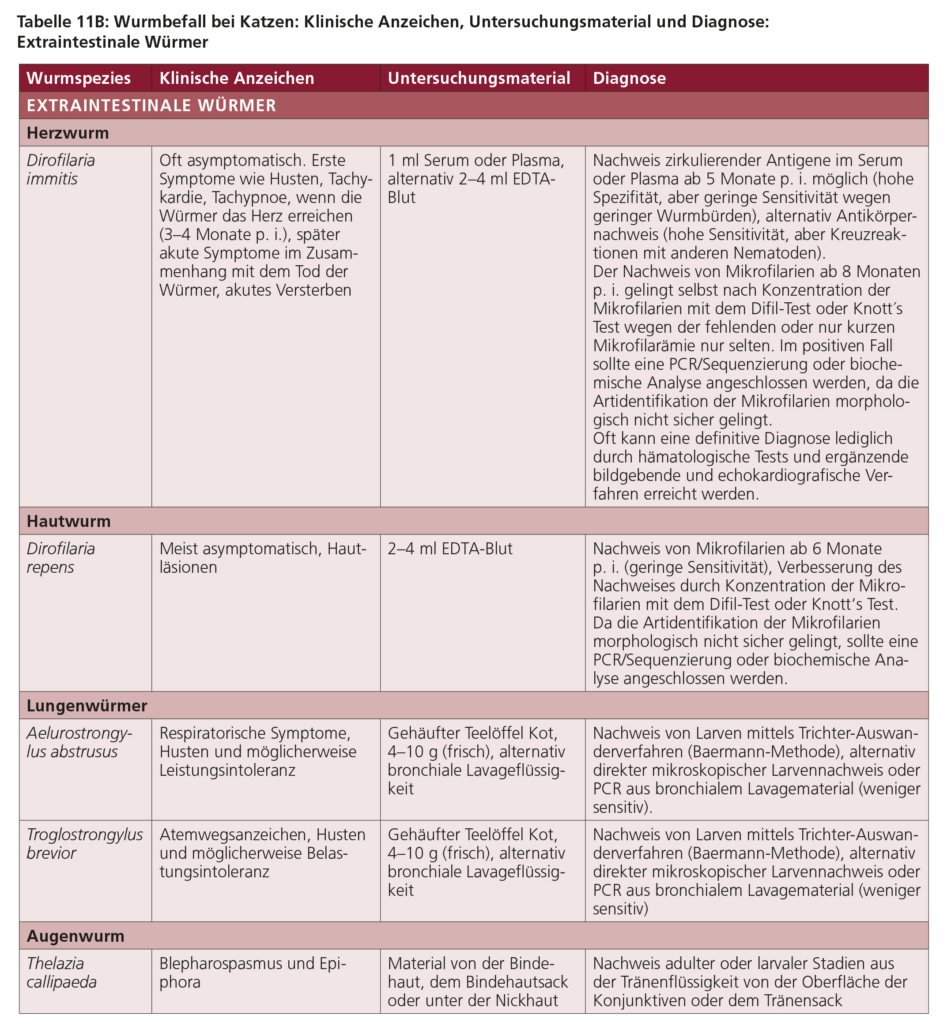
Extraintestinale Würmer:
- Herzwurm (Dirofilaria immitis)
- Hautwurm (Dirofilaria repens)
- Lungenwürmer (Angiostrongylus vasorum†, Crenosoma vulpis, Aelurostrongylus abstrusus)
- Augenwürmer (Thelazia callipaeda)
†Angiostrongylus vasorum wird manchmal auch als „französischer Herzwurm“ bezeichnet, was darauf zurückzuführen ist, dass sich die adulten Würmer in den Pulmonalarterien und nicht im Lungengewebe an sich befinden.
Diverse Details zu diesen Spezies der Hunde werden in den Tabellen 2A, 2B und 2C sowie der Katzen in den Tabellen 4A, 4B und 4C zusammengefasst. Einige dieser Parasiten haben eine größere Bedeutung als andere aufgrund
- ihrer Prävalenz,
- ihrer Pathogenität,
- ihres zoonotischen Potenzials oder
- einer Kombination dieser Gründe.
Im Sinne der besseren Lesbarkeit dieser ESCCAP-Empfehlung werden im Folgenden unter anderem Helminthen als „Würmer“, Medikamente zur Behandlung gegen Helminthen als „Anthelminthika“ und die Anwendung dieser als „Entwurmung“ bezeichnet.
Diese ESCCAP-Empfehlung umfasst Maßnahmen zur Diagnostik, Prävention, Metaphylaxe und Therapie von Wurminfektionen bei Hund und Katze, Maßnahmen zur Prävention einer Übertragung von Hund und Katze auf andere Tiere oder den Menschen, Maßnahmen zur Reduktion einer Umweltkontamination sowie Hinweise zur Information von TierhalterInnen.
Zielsetzung
Ziel dieser für Deutschland und Österreich adaptierten ESCCAP-Empfehlung ist es, einen aktuellen Überblick über die in Europa relevanten Helminthen (parasitische Würmer) zu geben sowie einen Schwerpunkt auf ihre Bedeutung innerhalb Deutschlands und Österreichs zu legen. Darüber hinaus werden konkrete Maßnahmen empfohlen, die Infektionen mit diesen Parasiten sowie Erkrankungen bei Tieren und/oder Menschen verhindern oder minimieren sollen.
Die vorliegende Empfehlung basiert auf aktuellen wissenschaftlichen Erkenntnissen. Teilweise sind weiterführende Studien notwendig, um umfassendere oder konkretere Aussagen zu bestimmten Teilaspekten machen zu können. ESCCAP sammelt in diesem Sinne weitergehende wissenschaftliche Studien und weist bis zu deren Ergebnissen in der vorliegenden Empfehlung auf noch offene Fragestellungen hin.
ESCCAP bietet evidenzbasierte, unabhängige Empfehlungen für TierärztInnen und TierhalterInnen für die Bekämpfung von Wurminfektionen bei Hunden und Katzen. Diese Leitlinie konzentriert sich auf die wichtigsten Gruppen von intestinalen sowie extraintestinalen Würmern.
Weitere Parasiten werden in anderen Leitlinien behandelt; auf diese wird im Text gegebenenfalls Bezug genommen. Weitere Informationen über die Kontrolle von Ektoparasiten, Dermatophyten, vektorübertragenen Krankheiten und intestinalen Protozoen finden Sie in den ESCCAP-Empfehlungen unter www.esccap.de/tieraerzte/empfehlungen/ oder www.esccap.org/guidelines/.
2. Aktuelle Situation und neue Bedrohungen
Es ist anzunehmen, dass durch die vermehrte Reisetätigkeit mit Haustieren sowie durch die klimatischen Veränderungen die derzeitige epidemiologische Situation bestimmter Endoparasiten in Europa beeinflusst bzw. verändert wird. So können z. B. bisher in Deutschland oder Österreich nicht vorkommende Parasiten hier eingeführt werden oder bisher seltene Krankheiten durch vermehrte Importe in derzeit nicht endemische Gebiete an Häufigkeit zunehmen. Darüber hinaus haben innerhalb der Europäischen Union die Abschaffung der Grenzkontrollen im Rahmen des Schengener Abkommens und die Umsetzung des PETS-Travel-Schemas im Vereinigten Königreich dazu geführt, dass Reisen zwischen den verschiedenen Ländern in Kontinentaleuropa problemlos möglich sind. Außer im Vereinigten Königreich gibt es keine oder nur begrenzte Zollkontrollen für Heimtiere, die von einem Land in ein anderes reisen.
Neben Haustieren, die mit ihren BesitzerInnen reisen, wird eine große Anzahl von Hunden und in geringerem Maße auch Katzen von Tierschutzorganisationen z. B. aus den Mittelmeerländern in Tierheime bzw. Privathaushalte in ganz Europa umgesiedelt. Dies ist von besonderer Bedeutung, da der Mittelmeerraum ein Gebiet ist, in dem Parasiten wie Dirofilaria immitis, als ein Beispiel für in Deutschland bisher nicht vorkommende Erreger, weit verbreitet sind.
Anwendung von Endoparasitika
Tierarzneimittel durchlaufen vor ihrer Zulassung durch europäische oder nationale Behörden einen strengen Prüfprozess und jede Anwendungsindikation muss wissenschaftlich begründet werden. TierärztInnen werden in der angemessenen Anwendung dieser Präparate gemäß der geltenden nationalen Gesetzgebung geschult. Die meisten modernen endoparasitiziden Präparate für Haustiere können metaphylaktisch oder therapeutisch zur Kontrolle von Endoparasiten eingesetzt werden. Dabei wirken die Präparate stets lediglich zum Zeitpunkt der Behandlung bzw. in den unmittelbar darauf folgenden Tagen, jedoch nicht vorbeugend/prophylaktisch für einen längeren Zeitraum.
3. Lebenslange Bekämpfung wichtiger Wurm-Arten
Wurmbefall wird durch vorbeugende Maßnahmen bzw. anthelminthische Behandlung kontrolliert. Nur wenige Parasiteninfektionen sind strikt altersabhängig; somit besteht auch mit zunehmendem Alter des Tieres das Risiko einer Infektion. Jedem Hund und jeder Katze sollte während des gesamten Lebens eine angemessene Wurmkontrolle zukommen.
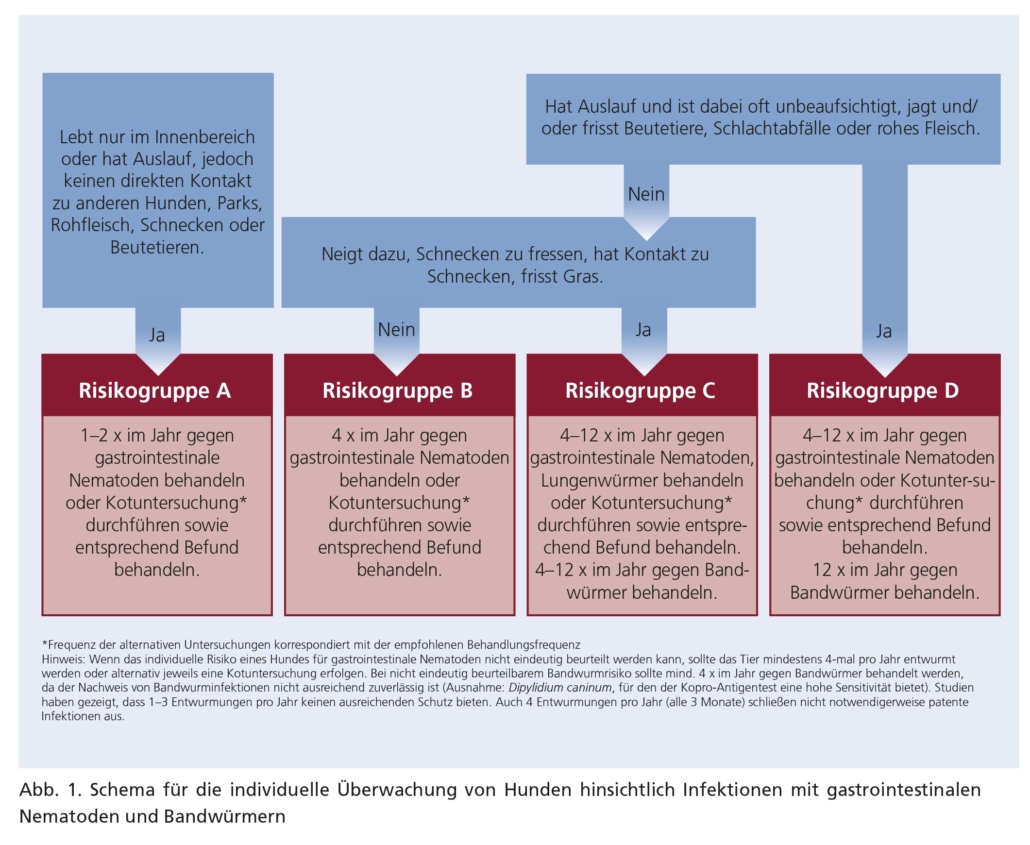
Die routinemäßige Behandlung und Vorbeugung von Wurminfektionen hängen von der jeweils geltenden Gesetzgebung, von den örtlichen und internationalen epidemiologischen Gegebenheiten und von individuellen Risikobewertungen, z. B. jagende Haustiere, frühere Lungenwurmexposition, Rohfleischernährung usw., ab. Das zoonotische Potenzial sowie seine Konsequenzen müssen ebenfalls berücksichtigt werden. Die Entwurmung sollte daher immer von einer Tierärztin/einem Tierarzt angeraten werden. Siehe Abbildungen 1 und 2: Schemata für die individuelle Entwurmung von Hunden und Katzen.
4. Strategische Bekämpfung von Wurmbefall
Wesentliche Maßnahmen bei der Bekämpfung von Wurmbefall bei Hunden und Katzen in Deutschland und Österreich sind:
- Tierärztlich verordnete Maßnahmen gegen Endoparasitenbefall bei Hund und Katze (Diagnostik, Medikation, Prävention)
- Hygienemaßnahmen, insbesondere regelmäßiges Entfernen von Hunde- und Katzenkot, um eine Kontamination der Umgebung mit infektiösen Parasitenstadien zu verringern
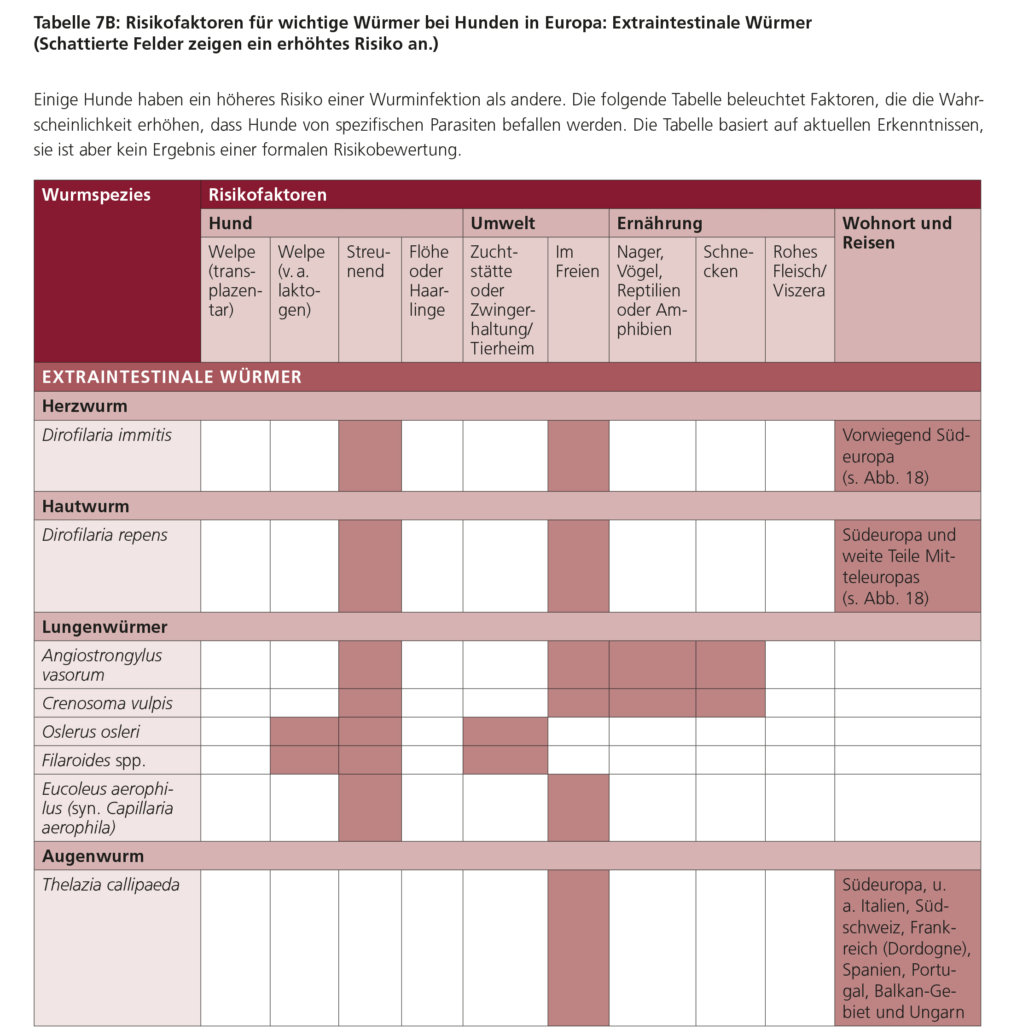
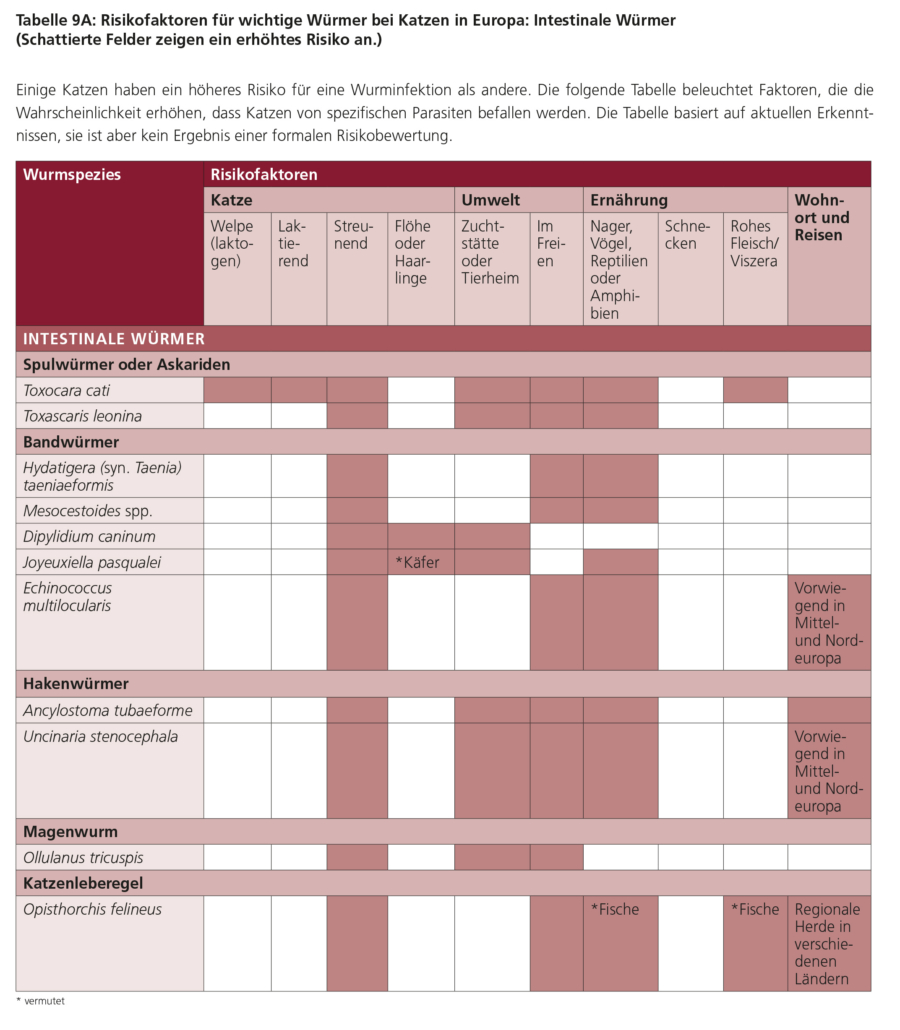
- Ernährung mit kommerziellen oder ausreichend erhitzten (10 Min., Kerntemperatur 65 °C) oder vorab gefrorenen (1 Woche, -17 bis -20 °C), selbst zubereiteten Futtermitteln, um Infektionen mit Parasiten, die durch rohes Fleisch, rohe Innereien oder rohen Fisch übertragen werden, zu vermeiden (siehe Tabellen 7 und 9)
- Vermeidung einer Aufnahme von Wildnagern, Kadavern, Schlachtabfällen usw.
- Koprophagie sollte verhindert werden, um Infektionen als Fehlwirt zu vermeiden (alveoläre Echinococcose)
- Angebot von frischem Trinkwasser (nicht aus Pfützen trinken lassen)
Auch wenn das Risiko eines Wurmbefalls bei Tieren bestimmter Altersstufen und Haltungsformen größer ist als bei anderen Tieren, ist bei Hunden und Katzen aller Altersstufen und Haltungsformen eine Infektion mit bestimmten Wurmarten möglich.
Eine anthelminthische Behandlung ist immer dann angezeigt, wenn bei Hund oder Katze ein Wurmbefall diagnostiziert wird. Voraussetzung für eine sachgerechte Behandlung ist die Identifikation des Parasiten. Einer Behandlung sollten entsprechende Maßnahmen zur Prävention folgen.
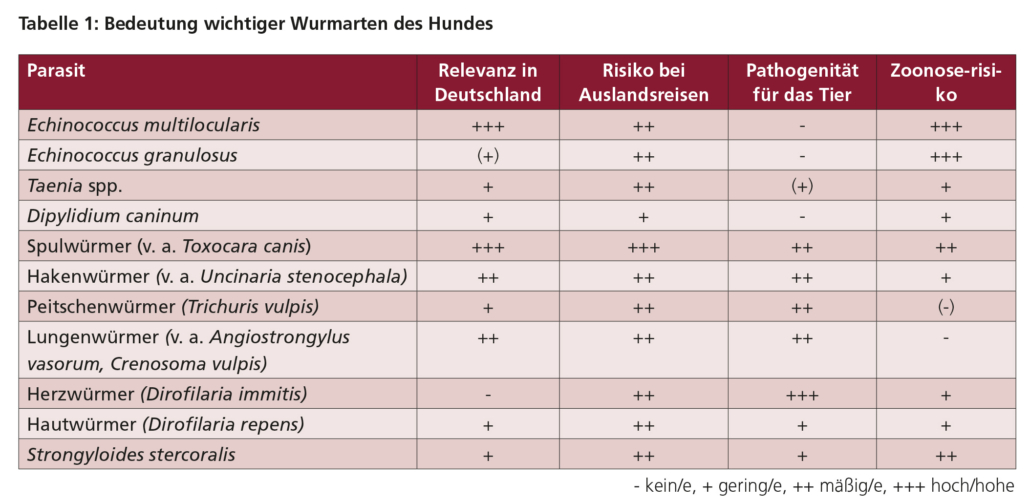
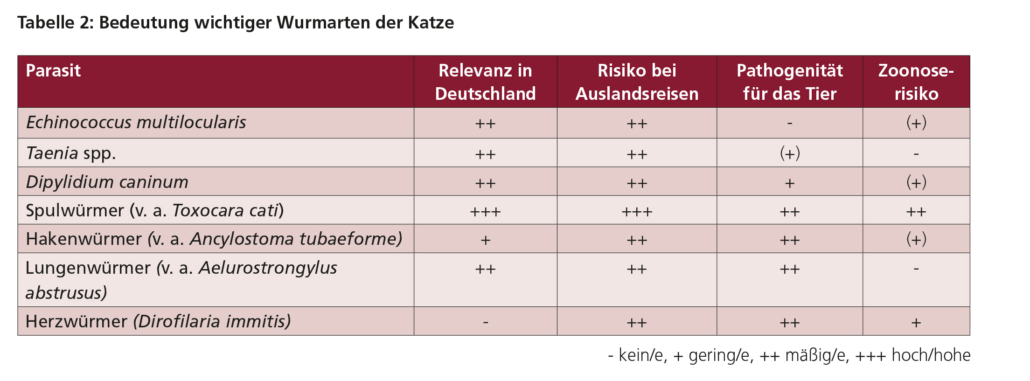
Verschiedene Helminthen stehen bei Hunden und Katzen innerhalb Deutschlands und Österreichs unterschiedlich stark im Fokus, je nachdem, ob sie schwerwiegende Erkrankungen hervorrufen können, ein Zoonoserisiko bergen oder eine hohe Prävalenz in Deutschland/Österreich und beliebten Reiseländern hiesiger TierhalterInnen aufweisen. In den untenstehenden Übersichten findet sich eine entsprechende Einteilung:
Für gesunde Hunde und Katzen ist die Vorbeugung von Wurminfektionen unerlässlich. Um die Präventionsmaßnahmen zu vereinfachen, hat ESCCAP drei „Schlüssel“-Parasitengruppen identifiziert, die schwere Krankheiten verursachen können, ein Zoonoserisiko darstellen und/oder in einigen oder allen Gebieten Europas stark verbreitet sind:
- Spulwürmer (Toxocara spp., in allen Gebieten weit verbreitet)
- Echinococcus spp. (zur Verbreitung siehe Abbildungen 9 und 10)
- Herz- und Lungenwürmer (Dirofilaria immitis, zur Verbreitung siehe Abbildung 18; Angiostrongylus vasorum tritt europaweit in endemischen Gebieten auf)
Spulwurminfektionen treten in ganz Europa auf, während die Verbreitung anderer Infektionen geografisch bedingt ist. Wenn man die Maßnahmen zur Spulwurmbekämpfung um die Bekämpfung von Echinococcus spp. und/oder D. immitis/A. vasorum ergänzt, können grundlegende Bekämpfungspläne für Hunde und Katzen in ganz Europa erstellt werden.
- In Gebieten wie Deutschland, in denen Echinococcus multilocularis endemisch ist, sollten Hunde, die kleine Beutetiere jagen und fressen können, monatlich mit einem gegen diesen Parasiten wirksamen Mittel behandelt werden.
- In Gebieten, in denen Echinococcus granulosus endemisch ist, sollten Hunde, die Zugang zu Innereien oder Tierkadavern haben, mindestens alle sechs Wochen mit einem gegen diesen Parasiten wirksamen Mittel behandelt werden.
- In Gebieten, in denen Dirofilaria spp. endemisch ist, wird die konsequente vorbeugende Verabreichung eines geeigneten Anthelminthikums während der Vektorsaison empfohlen. In Gebieten wie Deutschland und Österreich, in denen Angiostrongylus vasorum endemisch ist, verhindern regelmäßige Entwurmungen mit einem gegen diesen Parasiten wirksamen Anthelminthikum oder Kotuntersuchungen mit befundabhängiger Behandlung das Auftreten ausgeprägter klinischer Anzeichen.
- Bei Tieren, für die Toxocara spp. ein signifikantes Infektionsrisiko darstellen, wird eine mindestens viermalige Entwurmung oder Kotuntersuchung pro Jahr empfohlen.
Die Bekämpfung anderer Parasiten wie Hakenwürmer, Lungenwürmer und Peitschenwürmer kann bei Bedarf ergänzt werden.
Für alle Parasiten sollte eine geeignete strategische Anthelminthika-Behandlung ermittelt und die Tiere sollten in angemessenen Abständen behandelt werden. Alternativ können bei bestimmten Risikoszenarien eine regelmäßige Kotdiagnostik sowie andere Untersuchungen (z. B. Serologie) und Entwurmungen nach Befund durchgeführt werden. Die Wirksamkeit der eingesetzten Präparate sollte regelmäßig (d. h. mindestens 1 x jährlich) überprüft werden.
Ausführlichere Überlegungen zu den einzelnen Parasiten bei Haustieren finden Sie jeweils in den entsprechenden Abschnitten.
4.1 Entwurmung von Hunden
- Entwurmungsmaßnahmen sollten immer auf Anraten einer Tierärztin/eines Tierarzts durchgeführt werden. Bei den Risikogruppen A, B und C kann hinsichtlich der Kontrolle von Infektionen mit intestinalen Nematoden eine regelmäßige Kotuntersuchung (ggf. mit anschließender Entwurmung) eine gute Alternative zur strategischen Entwurmungsbehandlung sein. Die Kotuntersuchungen und ggf. serologische Tests sollten dabei in derselben Frequenz wie für die strategischen Entwurmungen empfohlen durchgeführt werden und mindestens einmal pro Jahr erfolgen.
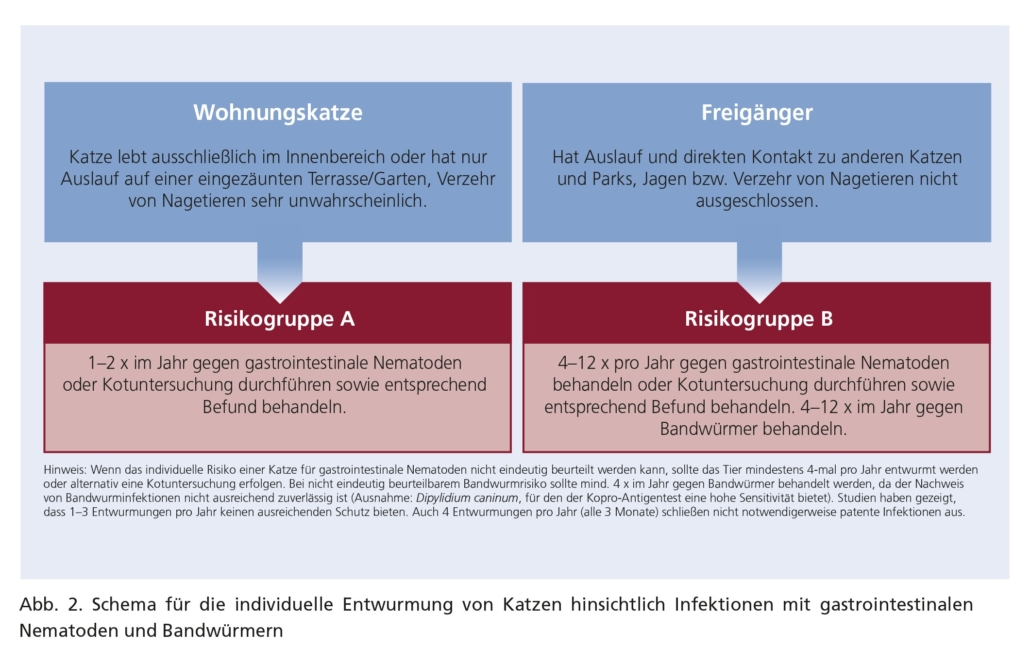
4.2 Entwurmung von Katzen
- Entwurmungsmaßnahmen sollten immer auf Anraten einer Tierärztin/eines Tierarzts hin durchgeführt werden. Bei den Risikogruppen A und B kann hinsichtlich der Kontrolle von Infektionen mit intestinalen Nematoden eine regelmäßige Kotuntersuchung (mit ggf. anschließender Entwurmungsbehandlung) eine gute Alternative zur regelmäßigen Entwurmung sein. Die Kotuntersuchungen sollten dabei in derselben Frequenz wie für die strategischen Entwurmungen empfohlen durchgeführt werden.
5. Biologie, Diagnose und Bekämpfung von Würmern
5.1 Spulwürmer (Toxocara spp., Toxascaris leonina)
Toxocara canis ist ein großer intestinaler Nematode, dessen adulte Stadien bis zu 15 cm lang werden können. Die Infektion mit T. canis führt vor allem bei Hundewelpen zu Krankheitserscheinungen. In ähnlicher Weise kann Toxocara cati, dessen adulte Exemplare bis zu 10 cm lang werden, bei Katzenwelpen eine Erkrankung verursachen. Im Gegensatz zu den beiden vorgenannten jeweils für Caniden bzw. Feliden spezifischen Spulwürmern tritt Toxascaris leonina sowohl bei Hunden als auch bei Katzen auf und ist zudem wechselseitig übertragbar. Dieser bis zu 12 cm lange Parasit kommt im Vergleich zu den Toxocara-Arten seltener vor und ist weniger pathogen.
Eine intestinale Infektion mit Toxocara spp. kann bei Hunde- und Katzenwelpen, aber auch bei älteren Hunden und Katzen auftreten. Menschen können sich durch die versehentliche Aufnahme von infektiösen Eiern oder den Verzehr von nicht ausreichend gekochtem Fleisch, das Larven enthält, infizieren.
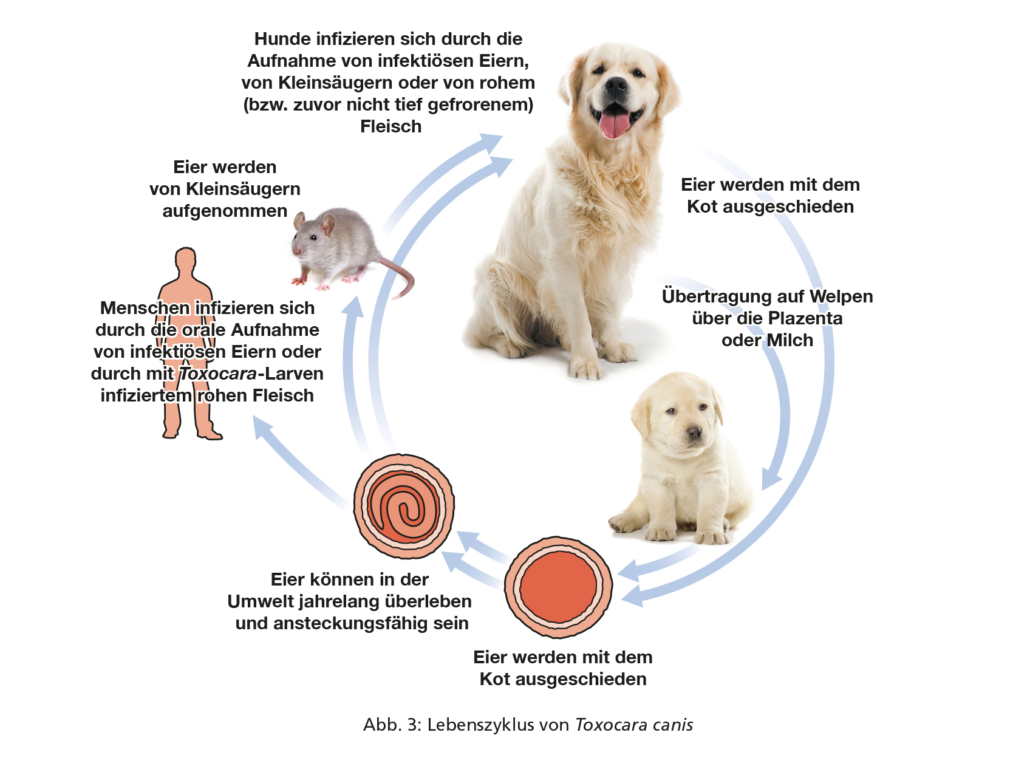
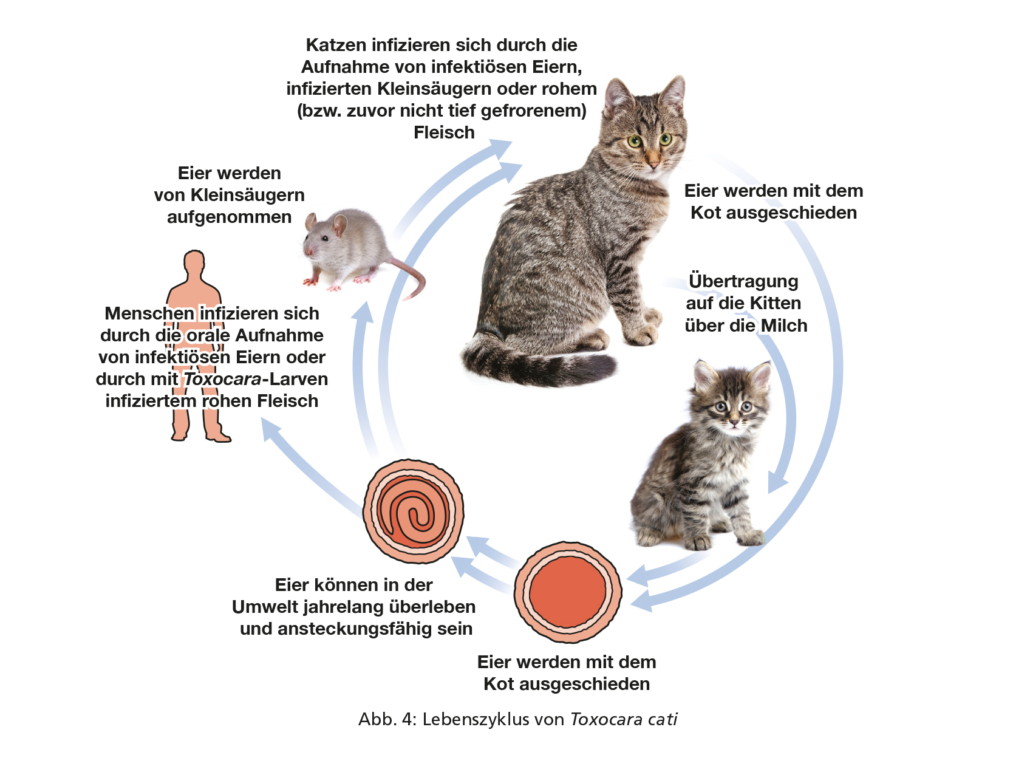
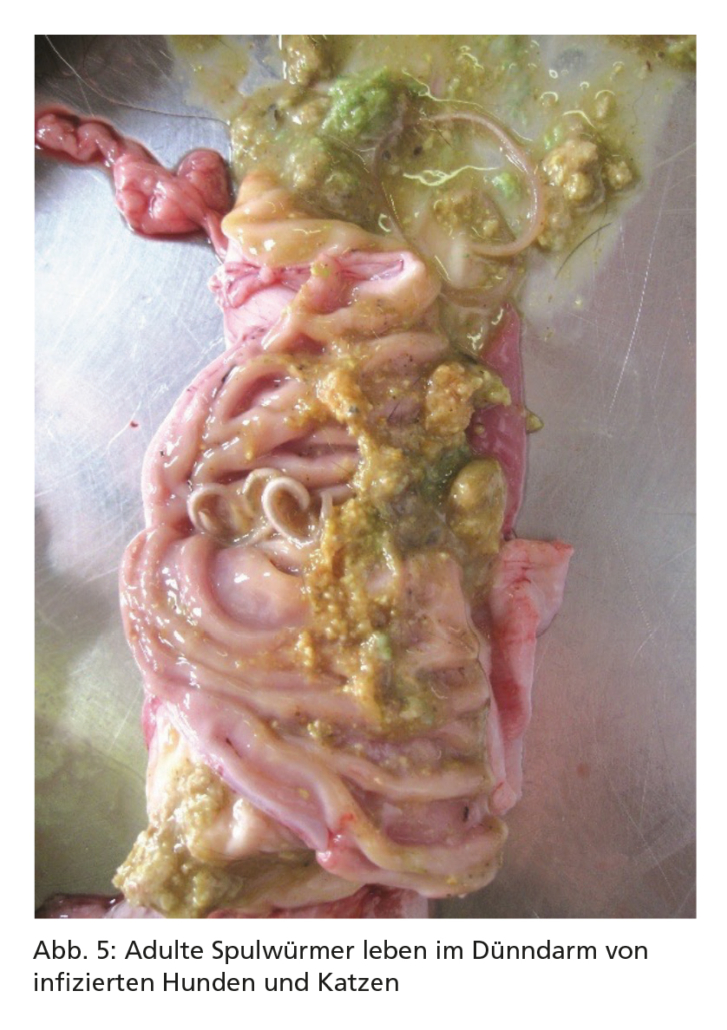
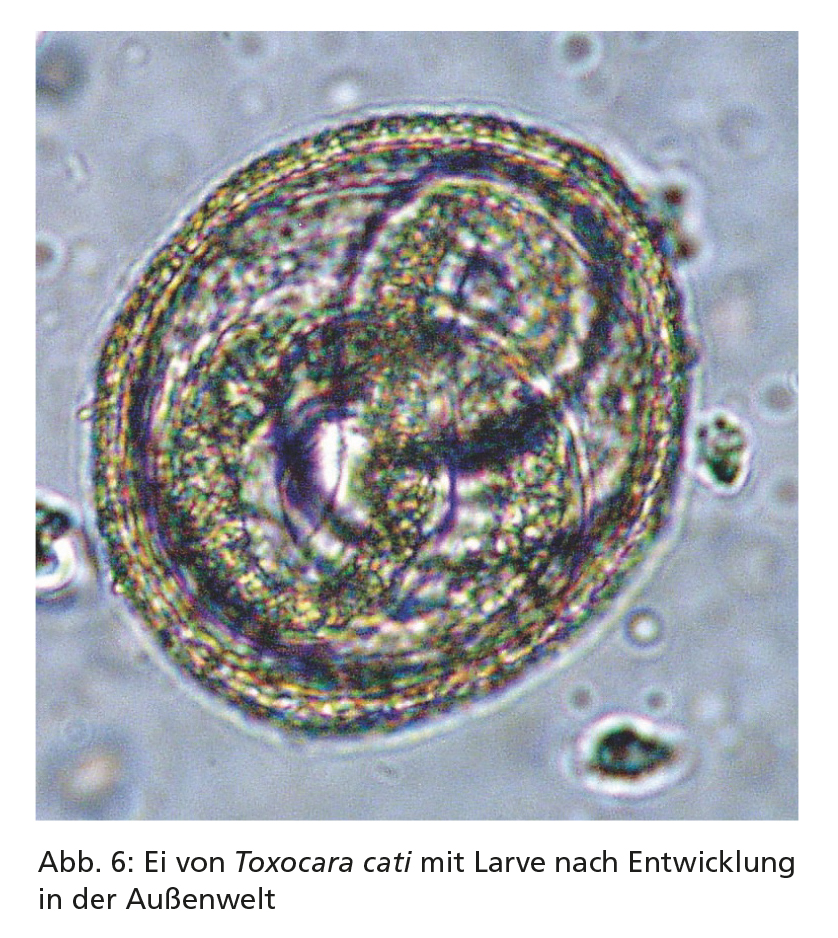
Adulte Würmer besiedeln den Dünndarm (Abb. 5), wo sie zahlreiche Eier legen, die dann mit dem Kot ausgeschieden werden. Im Ei entwickelt sich bei günstigen Umgebungsbedingungen (warm, feucht) in frühestens ca. zwei Wochen eine infektiöse Larve, die dort jahrelang überleben kann. Hunde und Katzen infizieren sich, wenn sie infektiöse Eier aus der Umwelt aufnehmen (Abb. 6). Zudem können sie sich infizieren, wenn sie nicht ausreichend gegartes bzw. nicht ausreichend gefrorenes Fleisch oder infizierte paratenische Wirte (z. B. Nagetiere) fressen.
Im Darm schlüpfen aus den Eiern Larven, die die Dünndarmwand durchdringen und (vor allem, was die Larven der Toxocara-Arten betrifft) anschließend eine hepatotracheale Wanderung durchlaufen. Diese ist abgeschlossen, wenn die Larven mit dem Flimmerepithel der Trachea zum Pharynx hochtransportiert, dann abgeschluckt werden und so in den Dünndarm zurückkehren (Abb. 3 und Abb. 4). Ein Teil der Larven gelangt jedoch nicht in den Darm, sondern vollzieht eine somatische Streuung mit Befall der Muskulatur oder anderen Geweben. Dort können sie als hypobiotische Larvenstadien symptomlos über Jahre überdauern. Bei infizierten trächtigen Hündinnen führt die Reaktivierung der hypobiotischen T. canis-Larven zur Infektion der Feten durch die Passage der Larven über die Plazenta ab etwa dem 42. Tag der Trächtigkeit. Zudem können Spulwurmlarven später über die Muttermilch auf die Welpen übertragen werden (Abb. 3). Katzenwelpen können nicht über die Plazenta, sondern lediglich über die Muttermilch infiziert werden (Abb. 4).
Bei Infektion mit T. leonina-Eiern erfolgt keine Körperwanderung, sondern nach einer Häutung der Larven in der Darmwand die Rückkehr ins Darmlumen und dort die Entwicklung zu geschlechtsreifen Stadien sowie nach ca. 7–10 Wochen die Eiausscheidung. Eine Körperwanderung kann in sogenannten paratenischen Wirten (z. B. Nager) erfolgen. Die somatische Migration kann auch bei Nicht-Caniden-/-Feliden-Wirten erfolgen, die dann als paratenische Wirte fungieren.
Des Öfteren treten auch bei erwachsenen Hunden und Katzen patente Spulwurminfektionen auf. Bei T. canis erfolgt die Eiausscheidung ca. 4–8 Wochen nach der Aufnahme infektiöser Eier (junge Hunde: 4–6 Wochen, ca. 1 Jahr alte Hunde: 6–8 Wochen), jedoch bereits ca. 3 Wochen nach der Geburt intrauterin sowie ab knapp 4 Wochen bei laktogen infizierten Welpen. Nach oraler Aufnahme infektiöser T. cati-Eier beträgt die Präpatenz hingegen mindestens 4, aber meistens ca. 8 Wochen. Auch nach Aufnahme paratenischer Wirte dauert es bis zu ca. einem Monat, bis T. canis- oder T. cati-Eier mit dem Kot ausgeschieden werden.
Intestinale Infektionen mit Spulwürmern der Gattung Toxocara kommen entsprechend sowohl bei Welpen als auch bei adulten Hunden und Katzen vor. Bei adulten Tieren führt ein Befall kaum zu klinischen Anzeichen, bei Welpen dagegen können Toxocara spp. schwere Erkrankungen hervorrufen.
Ob der Darm eines Tiers mit geschlechtsreifen Stadien befallen ist, lässt sich über regelmäßige Kotuntersuchungen klären. Dabei werden Flotationsverfahren angewendet, um die charakteristischen Spulwurmeier nachzuweisen. Seit einiger Zeit besteht zudem die Möglichkeit kommerzieller Kopro-Antigenverfahren (ELISA). Diese sind in der Lage, eine Toxocara-Infektion auch während der Prä- oder der Postpatenz nachzuweisen, und führen nicht zu einem falsch positiven Befund bei den Darm passierenden, koprophag aufgenommenen Toxocara-Eiern. Spulwürmer produzieren enorme Mengen an sehr langlebigen Wurmeiern. Infektionen mit diesen Parasiten verdienen wegen ihrer pathogenetischen sowie zoonotischen Bedeutung bei Hunden und Katzen über alle Altersstufen hinweg Beachtung.
Beim Menschen kann es nach oraler Aufnahme infektiöser Toxocara-Eier zu einer somatischen Wanderung der Larven (Larva migrans visceralis) kommen. Werden bei dieser somatischen Wanderung Auge, Nervenbahnen und/oder Gehirn des Menschen befallen, kann dies ernsthafte gesundheitliche Folgen haben (siehe Kapitel 9: „Prävention zoonotischer Parasitosen“).
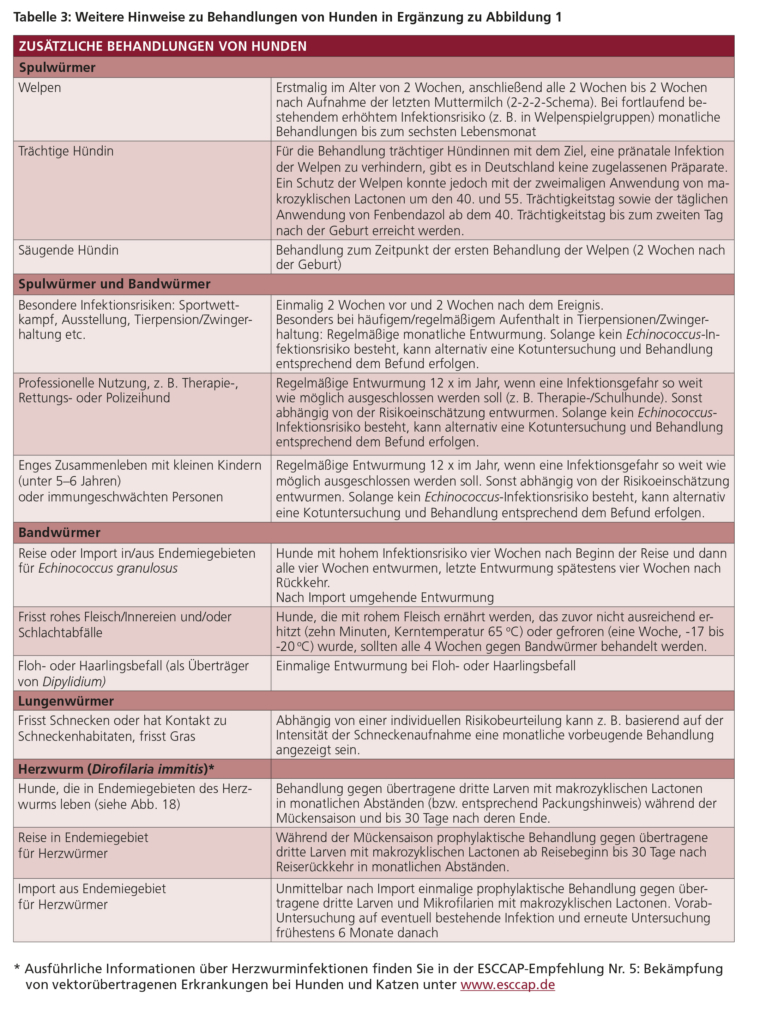
- Hundewelpen sollten ab einem Alter von 2 Wochen mit einem geeigneten Anthelminthikum behandelt werden. Anschließend wird die Behandlung in 2-wöchigen Abständen bis 2 Wochen nach dem Absetzen wiederholt. In Abhängigkeit vom Infektionsrisiko wird die Behandlung anschließend bis zum 6. Lebensmonat monatlich wiederholt.
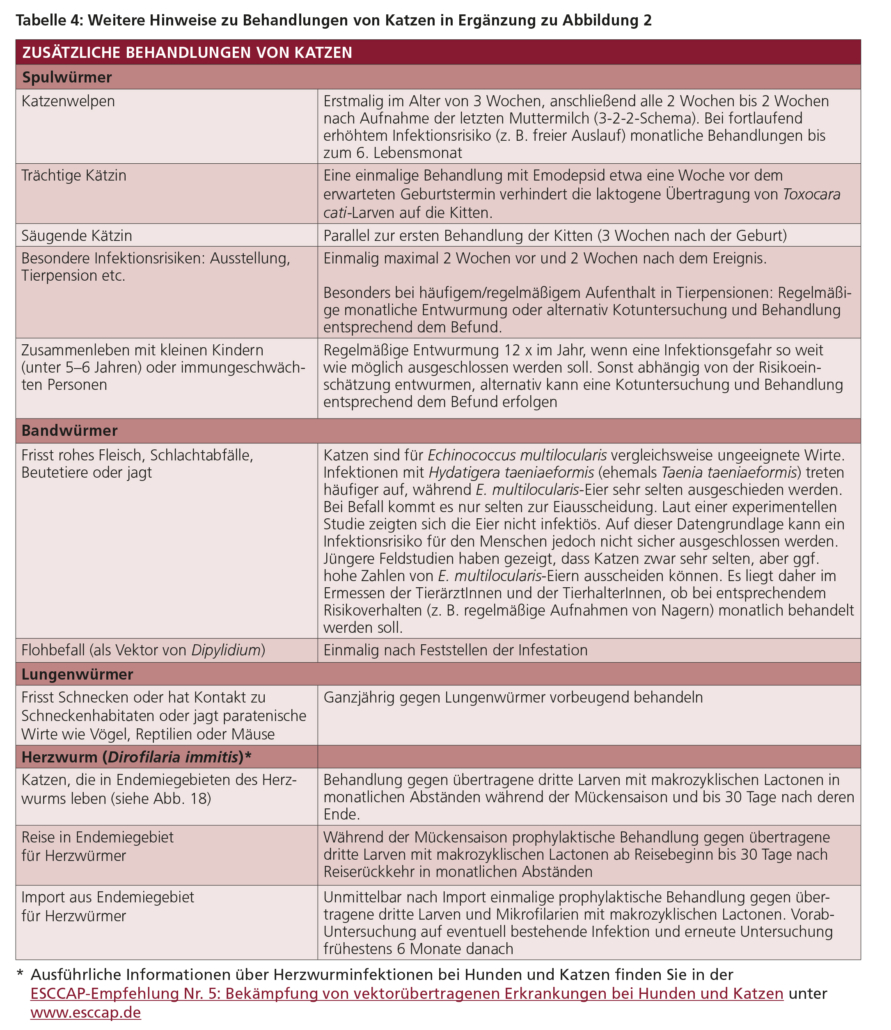
- Katzenwelpen sollten ab einem Alter von 3 Wochen mit einem geeigneten Anthelminthikum behandelt werden. Nach bisher vorliegenden Erfahrungen empfiehlt sich auch hier die fortlaufende Behandlung in 2-wöchigen Abständen bis 2 Wochen nach dem Absetzen. In Abhängigkeit vom Infektionsrisiko wird die Behandlung anschließend bis zum 6. Lebensmonat monatlich wiederholt.
- Für die Behandlung trächtiger Hündinnen mit dem Ziel, eine pränatale Infektion der Welpen zu verhindern, gibt es in Deutschland keine zugelassenen Präparate. Ein Schutz der Welpen konnte jedoch nachgewiesen werden mit z. B. der 2-maligen Anwendung von makrozyklischen Lactonen um den 40. und 55. Trächtigkeitstag bzw. der täglichen Anwendung von Fenbendazol ab dem 40. Trächtigkeitstag bis zum 2. Tag nach der Geburt.
- Trächtige Kätzinnen können etwa 7 Tage vor der voraussichtlichen Geburt mit einem emodepsidhaltigen Spot-on-Präparat behandelt werden, um eine laktogene Übertragung von T. cati-Larven auf die Kitten zu verhindern.
- Säugende Hündinnen und Kätzinnen sollten gleichzeitig mit der ersten Behandlung ihrer Nachkommen behandelt werden, da sie parallel zu ihren Welpen patente Infektionen entwickeln können.
Für adulte Hunde und Katzen stellt ESCCAP Folgendes fest:
- Über eine mindestens erforderliche Anzahl an Entwurmungen unter unterschiedlichen epidemiologischen Bedingungen stehen derzeit keine gesicherten Daten zur Verfügung. Ein- oder zweimalige Behandlungen pro Jahr haben jedoch in epidemiologischen Studien innerhalb der untersuchten Populationen im Durchschnitt keine ausreichende Wirkung gezeigt. Daher ist eine Behandlungsfrequenz von mindestens 4-mal pro Jahr eine allgemeine Empfehlung, falls das individuelle Infektionsrisiko unklar ist oder Infektionen nicht durch koproskopische Untersuchungen ausgeschlossen werden können.
- Gesichert ist, dass mit einer monatlichen Entwurmung eine Patenz von Toxocara spp. weitgehend ausgeschlossen werden kann, da die Präpatenz mindestens 4 Wochen beträgt. Eine monatliche Entwurmung kann daher in bestimmten Fällen – z. B. bei hohem Infektionsrisiko (zahlreiche Infektionsmöglichkeiten, regelmäßig unbeaufsichtigter Auslauf) und engem Kontakt in Familien mit Kleinkindern – angezeigt sein. Eine monatliche Entwurmung kann aus diesem Wissen heraus jedoch nicht pauschal empfohlen werden. Vielmehr gilt es, für jedes Tier eine individuelle Risikobewertung vorzunehmen und dann zu entscheiden, zu welchen Zeitpunkten eine Entwurmung bzw. ggf. eine Kotuntersuchung des betreffenden Patienten erfolgen soll.
- Zurzeit existieren für Europa keine wissenschaftlichen Nachweise für das Vorhandensein von Anthelminthika-Resistenz bei Spulwürmern von Hund und Katze. Bei Verdachtsfällen sollte zunächst Koprophagie oder ein Behandlungsfehler ausgeschlossen werden. Bei weiter bestehender Wurmeiausscheidung sollte erneut behandelt und durch Kotprobenuntersuchung ca. 14 Tage nach Behandlung der Erfolg überprüft werden.
Der exakte individuelle Infektionsstatus und der Erfolg der Behandlungen können nur über Kotuntersuchungen bzw. Kopro-Antigentests ermittelt werden. Allerdings ist zu berücksichtigen, dass es im Zeitraum zwischen diesen Untersuchungen jederzeit zu einer Ausscheidung von Wurmeiern kommen kann und dass niedrige Wurmeiausscheidungen bzw. Infektionsintensitäten mit einem falsch negativen Befund einhergehen können. Falsch positive koproskopische Kotbefunde treten relativ häufig bei Hunden auf, die Katzenkot mit Eiern von T. cati verzehrt haben, solche Fälle können jedoch mit weiteren Analysen (z. B. Kopro-Antigentests) abgeklärt werden.
Ohne Diagnostik lassen sich die individuelle Situation eines Tieres und die daraus resultierende empfohlene Entwurmungsfrequenz lediglich schätzen. Ist das Infektionsrisiko unbekannt oder können Infektionen grundsätzlich nicht durch diagnostische Untersuchungen ausgeschlossen werden, sind mindestens vier Behandlungen pro Jahr zu empfehlen.
Die ESCCAP-Schemata auf Seite 10 und 12 dieser Empfehlung dienen der Ermittlung individueller Kotuntersuchungs- bzw. Entwurmungsfrequenzen für einzelne Hunde und Katzen.
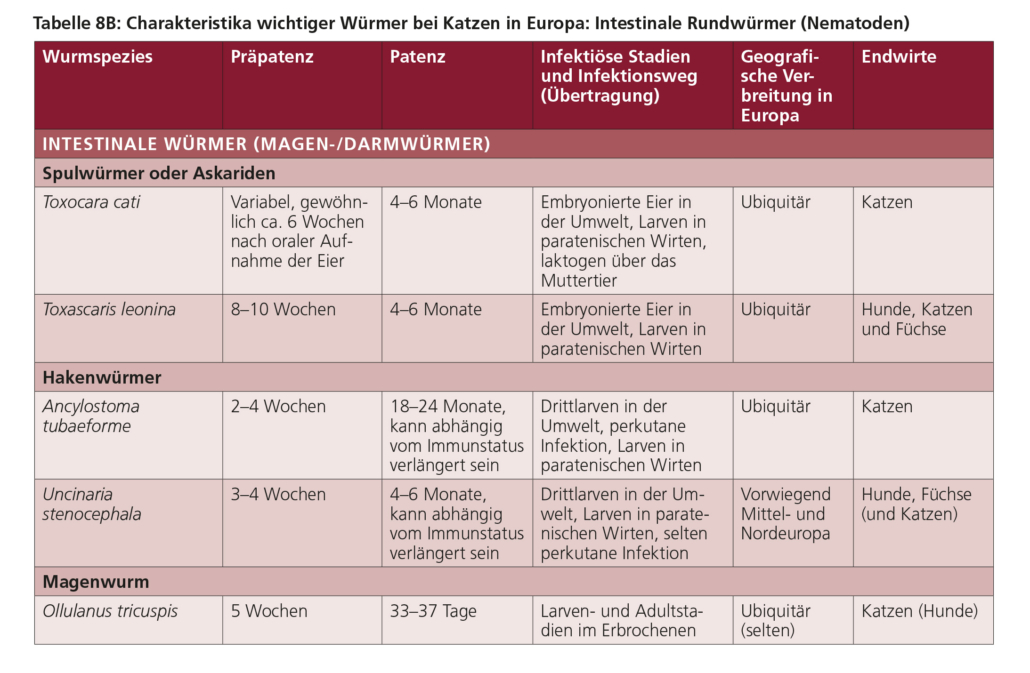
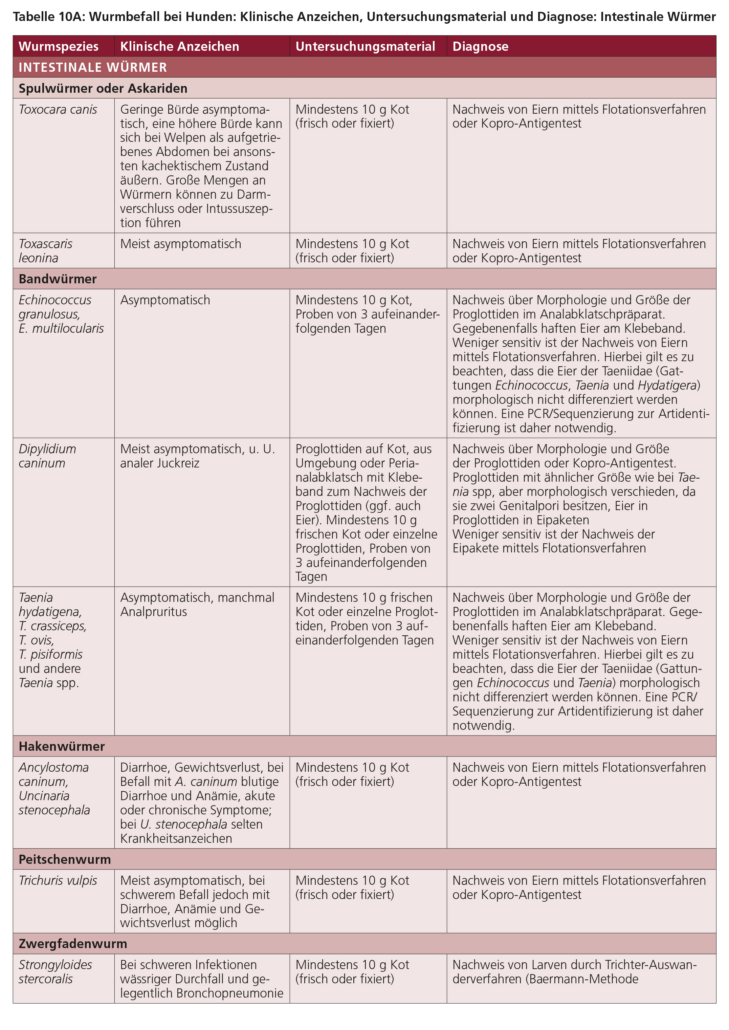
Weitere Informationen zu den Charakteristika von Toxocara spp., Risikofaktoren, klinischen Anzeichen, Diagnose und Behandlung finden Sie in den Tabellen 6B, 7, 8B und 9–11 sowie in der ESCCAP-Empfehlung Nr. 4 „Parasitological Diagnosis in Cats, Dogs and Equines“.
5.2. Bandwürmer
5.2.a. Echinococcus spp.
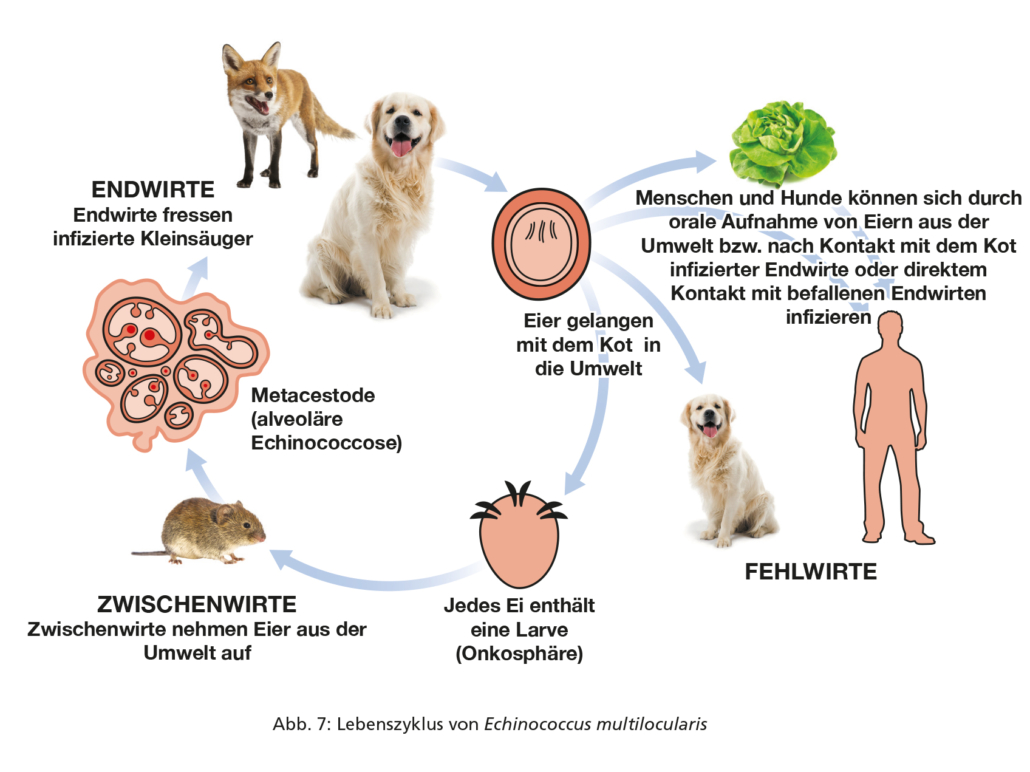
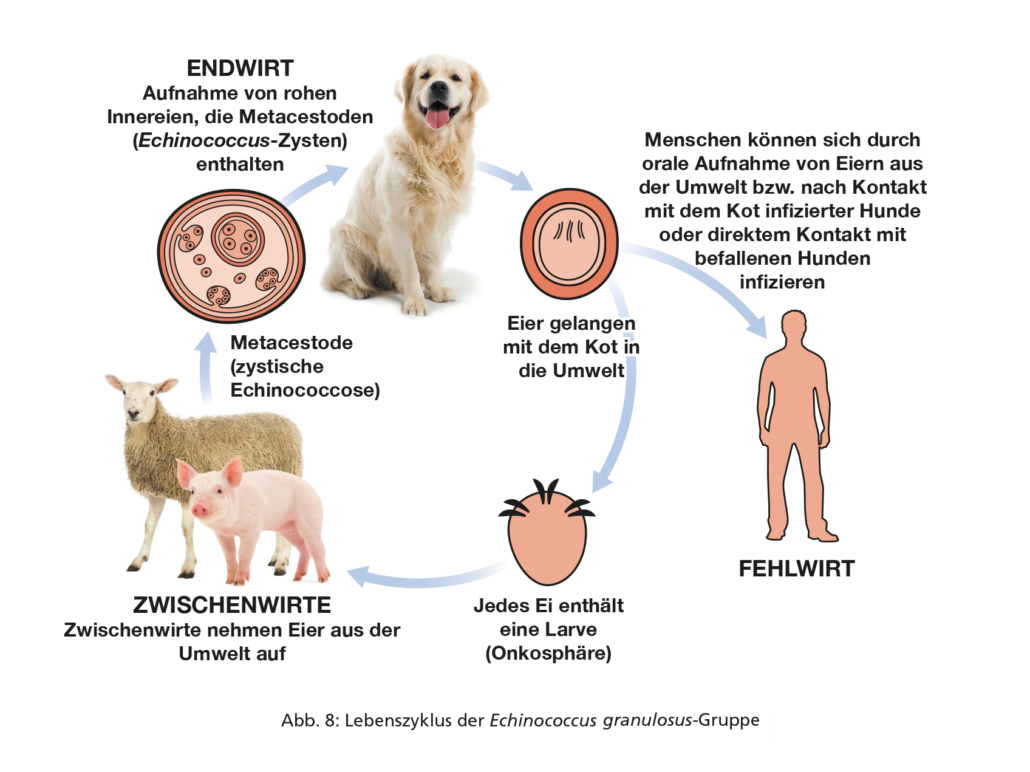
Echinococcus multilocularis (gefährlicher Fuchsbandwurm) ist ein kleiner Cestode, der den Dünndarm von Füchsen, Marderhunden, einigen anderen Caniden, jedoch selten von Hunden und sehr selten von Katzen bewohnt. Bei der Echinococcus granulosus-Gruppe (gefährlicher Hundebandwurm) handelt es sich ebenfalls um kleine Cestoden, die den Dünndarm von Hunden und einigen anderen Caniden, ausgenommen Füchsen, bewohnen. Die Lebenszyklen sind in den Abbildungen 7 und 8 dargestellt.
Beide Bandwürmer, E. multilocularis und die E. granulosus-Gruppe, bilden in Zwischenwirten extraintestinale Metacestodenstadien (Finnen) aus, und beide sind Zoonoseerreger, die für die öffentliche Gesundheit von großer Bedeutung sind. Beim Menschen verursacht E. multilocularis die alveoläre Echinococcose und die E. granulosus-Gruppe die zystische Echinococcose, die unbehandelt tödliche Folgen haben können. Beide Infektionen führen zur Bildung von Zysten, am häufigsten in der Leber (E. multilocularis, E. granulosus-Gruppe) oder in der Lunge (E. granulosus-Gruppe, aus dieser v. a. Echinococcus ortleppi, der sog. Rinderstamm). Diese entstehen nach der oralen Aufnahme von Eiern oder Proglottiden, die mit dem Kot der Endwirte ausgeschieden werden. Sie sind für Zwischen- bzw. Fehlwirte, einschließlich des Menschen, sofort infektiös. Auch der Hund kann sich auf diesem Wege infizieren und entsprechend eine alveoläre Echinococcose ausbilden.
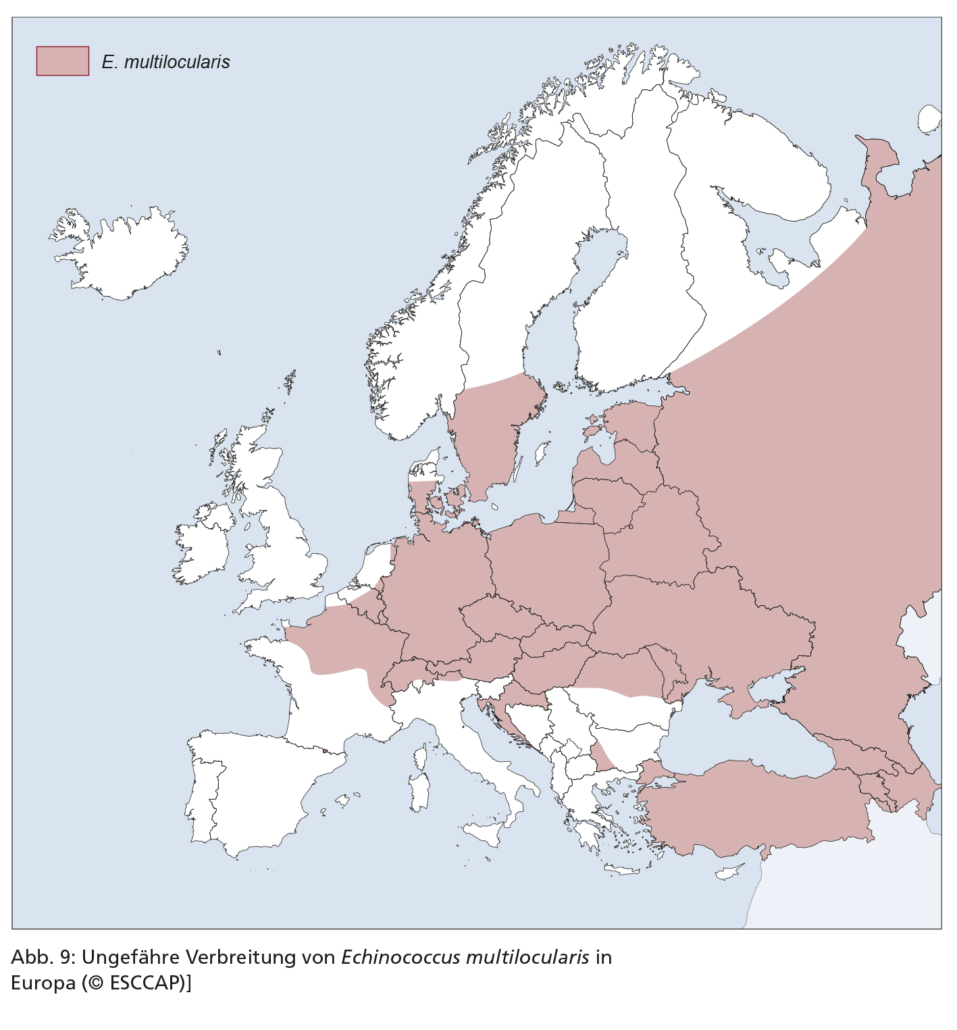
Echinococcus multilocularis ist in Zentral- und Osteuropa und damit in ganz Deutschland endemisch (Abb. 9). Hunde sind empfänglich für diesen Wurm, in geringerem Maße auch Katzen. In der Praxis steht der Befall von Hunden im Vordergrund, da Katzen als Wirte für E. multilocularis von untergeordneter Bedeutung sind und im Unterschied zu Hunden wahrscheinlich ein geringeres zoonotisches Risiko darstellen. Wichtigster Endwirt von E. multilocularis ist der Rotfuchs, natürliche Zwischenwirte sind Feldmäuse und andere Nagetiere. Die Infektion von Hund und Katze findet über den Verzehr wilder Nagetiere statt, die Metacestoden von E. multilocularis tragen. Die Präpatenz beträgt knapp 4 Wochen.
Hunde infizieren sich selten auch über die orale Aufnahme von E. multilocularis-Eiern als Fehlwirte, wobei es zur Entwicklung von Larvenstadien (Metacestoden) in inneren Organen (v. a. Leber) kommen kann. Gewöhnlich ergibt sich ein Verdacht auf das Vorliegen einer alveolären Echinococcose durch die Anwendung bildgebender Verfahren und lässt sich durch serologische, histologische oder molekularbiologische Untersuchungen abklären.
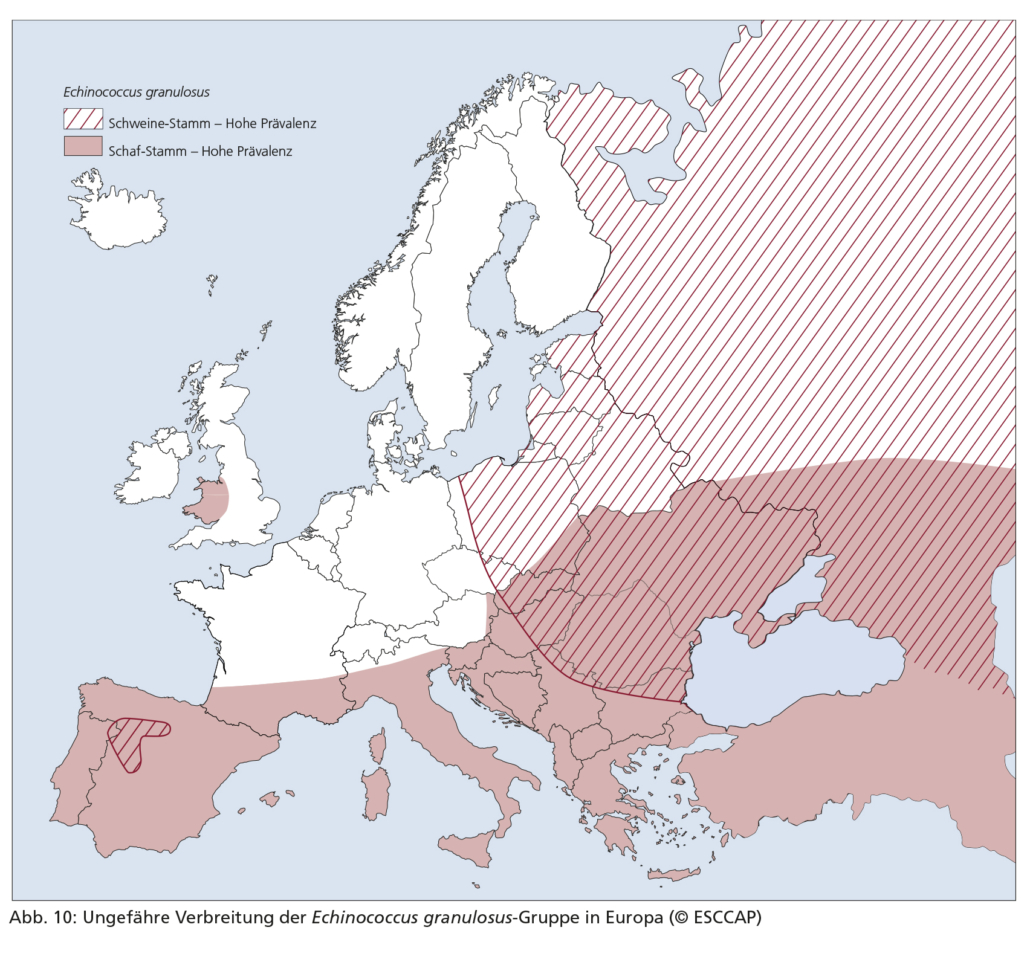
Die E. granulosus-Gruppe ist in Deutschland, Österreich und der Schweiz nur sehr selten anzutreffen. Wichtigster Hauptwirt ist der Hund. Die Infektion erfolgt vornehmlich über den Verzehr von Schlachtabfällen, Innereien oder Beutetieren, die Metacestoden der E. granulosus-Gruppe enthalten. In Deutschland werden diese Metacestoden bei Schlachttieren nur sehr selten aufgefunden (bei Rindern, selten auch Schweinen). Die Befallsrate bei Hunden liegt hierzulande nach neuesten Untersuchungen unter 0,3 % und spielt damit eine untergeordnete Rolle. Maßnahmen zur Bekämpfung dieses Wurmes beim Hund sind daher in Deutschland in der Regel nicht notwendig. Anders verhält es sich bei Hunden, die aus endemischen Gebieten (Abb. 10) importiert wurden oder dort auf Reisen waren/gehen. Die Präpatenz beträgt je nach Art 5–8 Wochen.
Echinococcus multilocularis und die Vertreter der Echinococcus granulosus-Gruppe sind Zoonoseerreger mit großer Bedeutung für die öffentliche Gesundheit. Die von den Endwirten über den Kot ausgeschiedenen Bandwurmeier sind unmittelbar infektiös. Infolge einer Infektion mit E. multilocularis oder Erregern der E. granulosus-Gruppe kommt es beim Menschen zu einer alveolären bzw. zystischen Echinococcose mit Zystenbildung in der Leber und/oder anderen Organen, die besonders im Fall einer E. multilocularis-Infektion unbehandelt meist tödlich verläuft. Die Infektion des Menschen erfolgt über die Aufnahme von Wurmeiern und/oder Proglottiden, die infizierte Tiere im Fell tragen oder mit dem Kot ausscheiden.
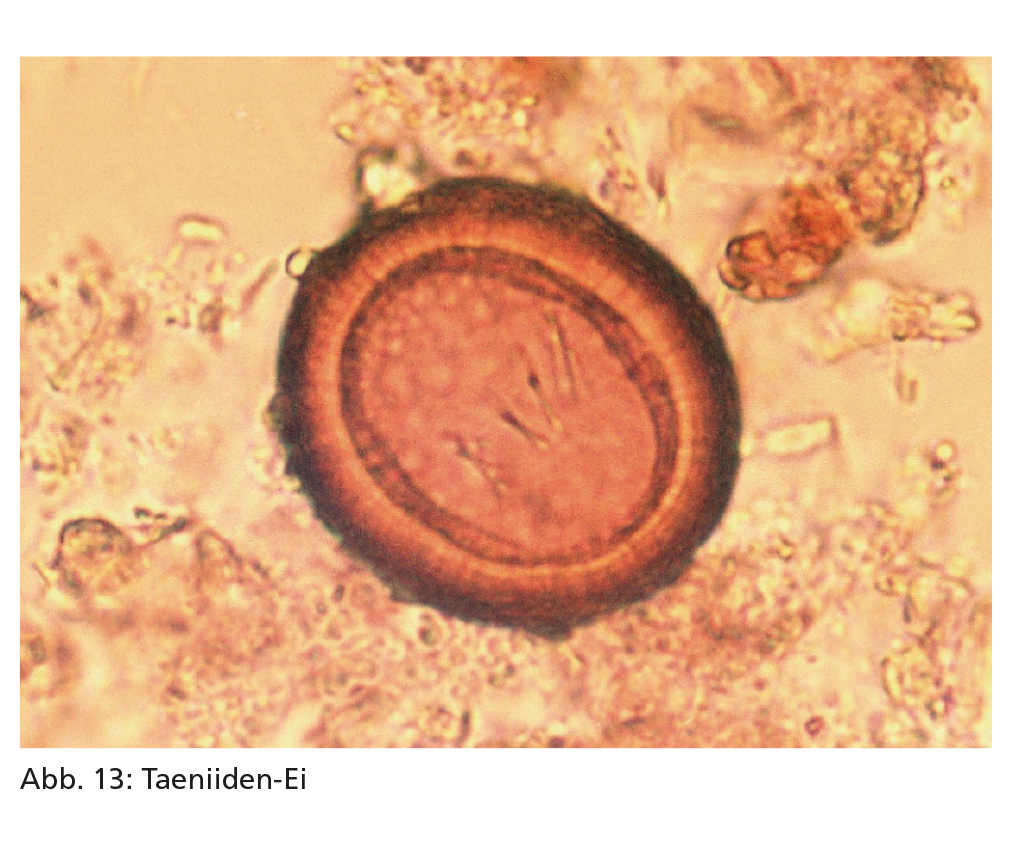
Die spezifische Diagnose einer Echinococcus-Infektion bei Hunden und Katzen ist schwierig, da die Eier der verschiedenen Taeniiden (Gattungen Echinococcus, Taenia und Hydatigera) im Rahmen von Kotuntersuchungen morphologisch nicht zu differenzieren sind. Die Echinococcus-Proglottiden sind außerdem so klein, dass sie im Kot mit bloßem Auge kaum zu erkennen sind. Zudem hat der mikroskopische Nachweis der Taeniiden-Eier (Abb. 13) mittels Flotationsverfahren nur eine geringe Sensitivität (Flotationslösungen mit höherer Dichte werden empfohlen, siehe Empfehlung Nr. 4 „Parasitological Diagnosis in Cats, Dogs and Equines“), da sie lediglich intermittierend im Kot auftreten. Alternativ kann man mit besserem Erfolg das „Perianalabklatsch mit Klebestreifen“-Verfahren durchführen.
In endemischen Echinococcus-Gebieten, also auch in ganz Deutschland, sollten koproskopisch nachgewiesene Taeniiden-Infektionen daher stets als potenzielle Echinococcus-Infektionen betrachtet und zur Abklärung eine PCR durchgeführt werden. In der Praxis heißt dies, dass jeder Nachweis von Taeniiden-Eiern bei Hund und Katze unbedingt weiter einer Abklärung auf eine Echinococcus-Infektion bedarf, da die Eier unmittelbar infektiös sind. Der Verdacht auf das Vorliegen einer alveolären Echinococcose entsteht in der Regel nach Anwendung bildgebender Verfahren und kann mittels serologischer, histologischer sowie molekularer Verfahren abgeklärt werden.
PRÄVENTION
Sofern umsetzbar, sollten Hunde keinen Zugang zu wilden Nagetieren haben. Koprophagie bei Hunden sollte unterbunden werden, um alveolärer Echinococcose vorzubeugen.
Hunde sollten kein unbehandeltes rohes Fleisch oder Schlachtabfälle erhalten, sondern ausschließlich mit kommerziellem Futter oder ausreichend erhitzter (10 Minuten, Kerntemperatur 65 °C) bzw. zuvor gefrorener (1 Woche, -17 bis -20 °C), selbst zubereiteter Nahrung gefüttert werden. Hunde, die nicht entsprechend vorbereitetes rohes Fleisch erhalten, sollten alle vier Wochen gegen Bandwürmer behandelt werden.
Für Hunde mit hohem Infektionsrisiko für E. multilocularis, die z. B. jagen, anderweitig Zugang zu wilden Nagetieren haben, Aasfresser sind (z. B. von toten Nagern) oder regelmäßig unbeaufsichtigten freien Auslauf haben, empfiehlt ESCCAP eine monatliche Entwurmung mit einem geeigneten Anthelminthikum.
Hunde, die in Echinococcus-Endemiegebiete im Ausland reisen und dort ein entsprechendes Infektionsrisiko haben, sollten vier Wochen nach Beginn der Reise und anschließend in 4-wöchigen Abständen bis vier Wochen nach Rückkehr mit einem geeigneten Anthelminthikum behandelt werden.
Hunde, die aus Echinococcus-Endemiegebieten importiert werden und dort ein entsprechendes Infektionsrisiko hatten, sollten umgehend mit einem geeigneten Anthelminthikum behandelt werden.
Für Katzen gelten grundsätzlich – bzw. aufgrund des stärker ausgeprägten Nagerfangverhaltens – die für Bandwurminfektionen relevanten Infektionsrisiken. Katzen sind jedoch für Echinococcus multilocularis vergleichsweise weniger geeignete Wirte (und keine Wirte der Echinococcus granulosus-Gruppe) und scheiden bei einem Befall mit E. multilocularis nach einer experimentellen Untersuchung nur in Einzelfällen und selbst dann meist nur geringe Eizahlen aus, zudem zeigten sich die ausgeschiedenen Eier für Nager als nicht infektiös. Allerdings wurden in jüngeren französischen Untersuchungen in Katzenkot zwar sehr selten, allerdings teilweise erhebliche Zahlen von möglicherweise infektiösen Eiern ermittelt. Aufgrund des gegenwärtigen Wissensstands ist somit ein Zoonoserisiko nicht ausgeschlossen, und es bleibt daher im Ermessen der verantwortlichen TierärztInnen sowie der TierhalterInnen, ob angesichts der individuellen Situation (z. B. Kleinkinder im Haushalt, sehr enger Kontakt zur Katze) dennoch in 4-wöchigen Intervallen behandelt werden soll.
MEDIKATION UND BEGLEITENDE MASSNAHMEN
Bei nachgewiesenem Echinococcus-Befall werden die TierhalterInnen über das bereits zuvor bestandene Infektionsrisiko informiert und über mögliche Nachweismöglichkeiten einer Infektion (z. B. bildgebende und serologische Diagnosemöglichkeit) instruiert. Die Hunde werden in der Praxis/Klinik sofort gebadet (Schutzkleidung inkl. Mundschutz!), zweimal im Abstand von 24 Stunden mit Praziquantel oder Epsiprantel behandelt und anschließend noch einmal gebadet. Die Hunde sind unter entsprechend strikten Hygienevorkehrungen bis 72 Stunden nach der zweiten Behandlung stationär aufzunehmen, da im Zuge der Behandlung hohe Mengen an Proglottiden und damit infektiöse Eier abgehen, die durch Anthelminthika nicht abgetötet werden. Der Kot ist über drei Tage dicht verpackt über den Hausmüll (der in der Müllverbrennung mündet) zu entsorgen. Der Erfolg der Therapie wird nach 7–14 Tagen durch eine PCR-Untersuchung des Kots kontrolliert.
Hunde können auch Fehlwirte für E. multilocularis werden, ohne Eier auszuscheiden, wenn sie Eier oder Proglottiden aus der Umwelt aufnehmen bzw. koprophagisches Verhalten zeigen. Dies führt zur Entwicklung von Metacestoden in Organen, primär der Leber. Solche Fälle sind selten, werden aber möglicherweise auch unterschätzt. Die Verdachtsdiagnose alveoläre Echinococcose wird bei Hunden in der Regel nach bildgebenden Verfahren gestellt und kann mit serologischen, histologischen und molekularen Methoden abgeklärt werden.
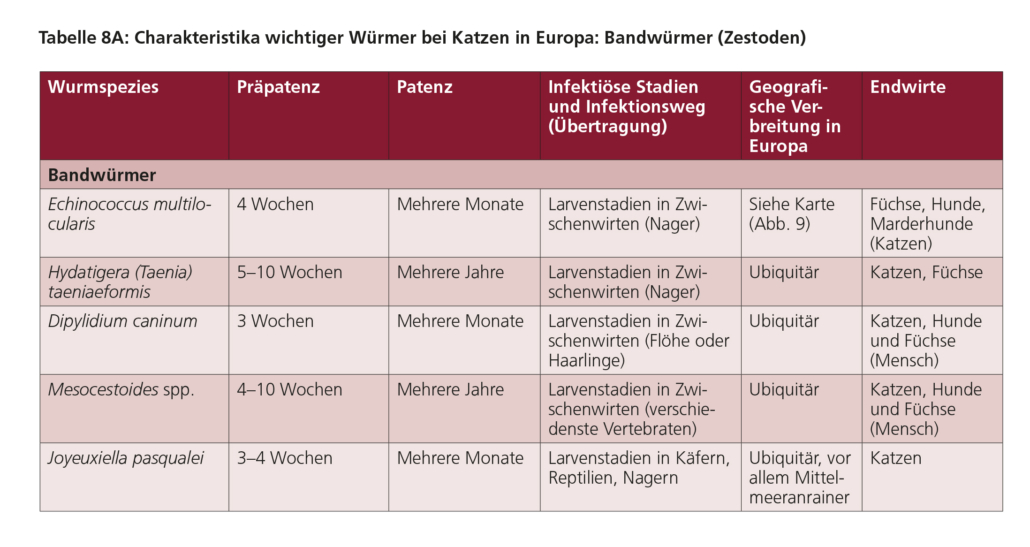
Weitere Informationen über Charakteristika, Risikofaktoren, klinische Anzeichen, Diagnose und Behandlungen von Echinococcus spp. finden Sie in den Tabellen 6A, 7, 8A und 9–11 sowie in der ESCCAP-Empfehlung Nr. 4 „Parasitological Diagnosis in Cats, Dogs and Equines“.
5.2.b. Dipylidium caninum
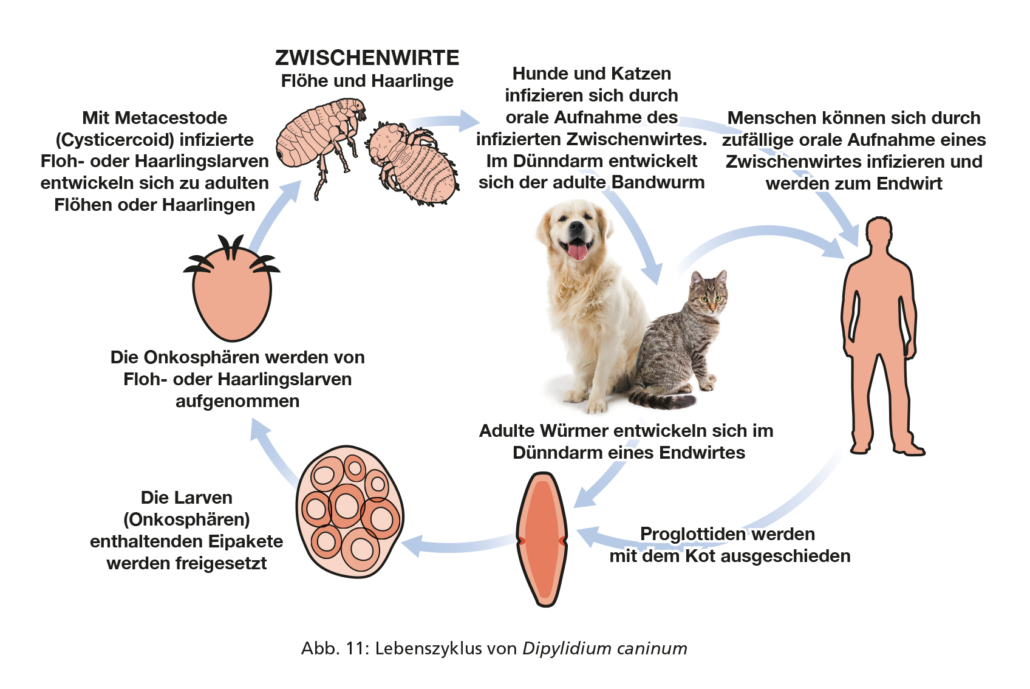
Dipylidium caninum ist ein Bandwurm, der Hunde und Katzen befällt und oft als Gurkenkernbandwurm bezeichnet wird. Zwischenwirte dieses Bandwurms sind Flöhe und Haarlinge. Die Infektion erfolgt durch orale Aufnahme infizierter Zwischenwirte. Der adulte Bandwurm entwickelt sich im Dünndarm des Endwirts (Abb. 11). Der adulte Bandwurm kann sich auch beim Menschen etablieren. Die Präpatenz beträgt zwei bis drei Wochen.
Infektionen gehen bei Hunden und Katzen nur selten mit klinischen Anzeichen wie Analpruritus („Schlittenfahren“) einher. Allerdings können massive Wurmbürden zu Dünndarmobstruktionen sowie insbesondere bei jungen Tieren zu Inappetenz oder Diarrhoe führen.
Die koproskopische Untersuchung, d. h. die Flotation zum Nachweis von Eipaketen, zur Diagnose eines Bandwurmbefalls ist sehr unsicher. Gelegentlich können die ca. 1 cm langen weißen Proglottiden aktiv aus der Afteröffnung auswandern, ansonsten werden sie mit dem Kot ausgeschieden. Proglottiden können auch im Fell des Analbereichs oder auf dem Schlafplatz des Tiers gefunden werden. Im frischen Zustand ähneln sie Gurkenkernen, im trockenen Zustand nehmen sie die Form von Reiskörnern an. Seit kurzem steht für den Nachweis der D. caninum-Infektion ein kommerzieller Kopro-Antigentest zur Verfügung, der eine wesentlich höhere Sensitivität als der koproskopische Wurmnachweis hat.
Dipylidium caninum-infizierte Hunde und Katzen werden mit einem zestodizid wirkenden Anthelminthikum (z. B. Praziquantel oder Epsiprantel) erfolgreich behandelt. Um Reinfektionen zu vermeiden, sollte eine begleitende Flohbehandlung bzw. -bekämpfung vorgenommen werden.
Durch regelmäßigen Einsatz eines gegen Flöhe bzw. Haarlinge wirksamen Präparats wird ein Dipylidium-Befall effektiv verhindert. In den USA ist über einzelne Fälle von Anthelminthika-Resistenz berichtet worden.
Weitere Informationen zu den Charakteristika von D. caninum, Risikofaktoren, klinischen Anzeichen, Diagnose und Behandlung finden Sie in den Tabellen 6A, 7, 8A und 9–11.
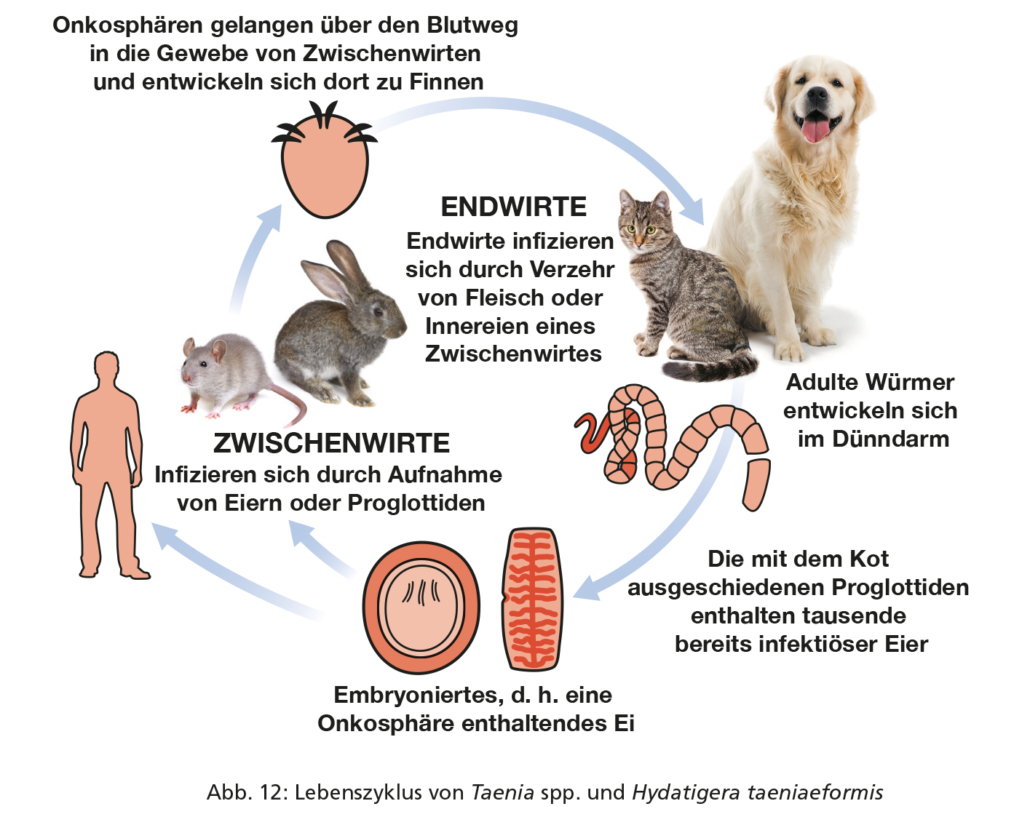
5.2.c. Taenia spp. und Hydatigera taeniaeformis
Taenia spp. und Hydatigera taeniaeformis sind „große“ Bandwürmer von Caniden und Feliden als Endwirte. Sie sind je nach Art etwa 20–250 cm lang. Bandwürmer dieser Gattungen kommen in allen europäischen Ländern vor.
Hunde und Katzen infizieren sich durch Verzehr von Fleisch oder Innereien befallener Zwischenwirte. Die Infektion der Zwischenwirte erfolgt durch orale Aufnahme von Bandwurmeiern, die über den Kot vom Endwirt ausgeschieden werden (siehe Abbildung 12).
Adulte Bandwürmer leben im Dünndarm der Endwirte einige Monate bis Jahre.
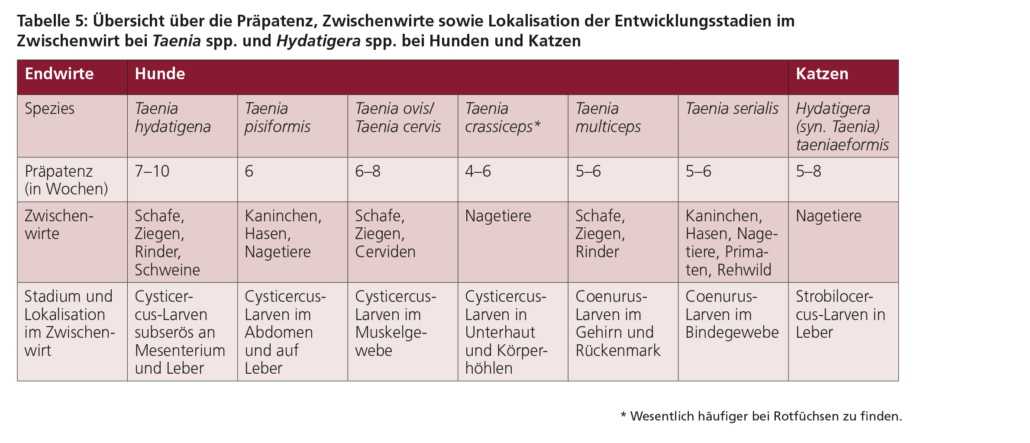
Die bei Caniden und Feliden vorkommenden Taenia– und Hydatigera-Arten haben je nach Art verschiedene Zwischenwirte (siehe Tabelle 1): Hydatigera (syn. Taenia) taeniaeformis (Nagetiere; Leber), Taenia crassiceps (Nagetiere; Unterhaut, Körperhöhlen), Taenia pisiformis (Hasenartige und Nagetiere; Leber), Taenia hydatigena (kleine Wiederkäuer, Rinder, Schweine; subserös an Mesenterium und Leber), Taenia ovis/Taenia cervi (Schaf, Ziege, Cerviden; Muskulatur), Taenia multiceps (Schaf, Ziege, Rinder; Gehirn und Rückenmark), Taenia serialis (Hasenartige; Bindegewebe).
Die Präpatenz für Taenia spp. reicht je nach Art von etwa vier bis neun Wochen bei Hunden und beträgt etwa 5–8 Wochen für Hydatigera (syn. Taenia) taeniaeformis bei Katzen. Die Patenz kann mehrere Monate bis zu mehrere Jahre andauern. Zum Beispiel kann T. ovis, eine Taenia-Art, die Hunde infiziert, bis zu fünf Jahre lang im Endwirt überleben.
Intestinaler Taenia- oder Hydatigera-Befall führt selten zu klinischen Anzeichen. Das aktive Auswandern von Proglottiden aus dem After kann gelegentlich zu Analjucken führen („Schlittenfahren“).
Taenia crassiceps verursacht selten exogene Vorwölbungen aufgrund subkutaner Zysten, diese können auch im Abdomen vorkommen.
Die koproskopische Untersuchung zur Diagnose eines Taenia- oder Hydatigera-Befalls ist sehr unsicher, und die Proglottiden werden oft nur zufällig makroskopisch beobachtet. Zudem hat der mikroskopische Nachweis der Taeniiden-Eier (Abb. 13) mittels Flotationsverfahren eine geringe Sensitivität (siehe Echinococcus). Dies gilt insbesondere, falls Flotationslösungen mit geringer Dichte verwendet werden (s. Guideline Nr. 4, Parasitological Diagnosis in Cats, Dogs and Equines). Alternativ kann man mit besserem Erfolg das Perianalklebestreifen-Verfahren durchführen.
Mikroskopisch lassen sich Taenia- bzw. Hydatigera-Eier nicht von Echinococcus-Eiern unterscheiden. Daher sollte jeder Nachweis von Taeniiden-Eiern im Kot als eine potenzielle Echinococcus-Infektion angesehen und zur Abklärung eine PCR durchgeführt werden. In der Praxis heißt dies, dass jeder Nachweis von Taeniiden-Eiern bei Hund und Katze unbedingt weiter einer Abklärung auf eine Echinococcus-Infektion bedarf, da die Eier unmittelbar infektiös sind.
Taenia- bzw. Hydatigera-infizierte Hunde und Katzen können mit einem zestodizid wirkenden Anthelminthikum (z. B. Praziquantel, Epsiprantel) erfolgreich behandelt werden. Eier können längere Zeit in der Umwelt überleben. Hunden sollten keine zuvor nicht ausreichend lang und tief gefrorenen (1 Woche, -17 bis -20 °C) rohen Innereien bzw. Fleisch als Futter angeboten werden. Der Verzehr von Kleinsäugern und anderen Zwischenwirten sollte bei Hunden und Katzen unterbunden werden (z. B. kein Zugang zu Jagdabfällen) bzw. TierhalterInnen sollten versuchen, ihre Hunde und Katzen von den verschiedenen Zwischenwirten fernzuhalten. Falls dies nicht möglich ist, sollten Hunde und Katzen in 4-wöchigen Zeitabständen behandelt werden.
Weitere Informationen über die Taenia spp.- und Hydatigera taeniaeformis-Risikofaktoren, klinische Anzeichen, Diagnose und Behandlungen finden Sie in den Tabellen 6A, 7, 8A und 9–11 sowie in der ESCCAP-Empfehlung Nr. 4 Parasitological Diagnosis in Cats, Dogs and Equines.
5.3. Herzwurm (Dirofilaria immitis)* und Hautwurm (Dirofilaria repens)
*Für Informationen über Angiostrongylus vasorum, den „französischen Herzwurm“, siehe Kapitel Lungenwürmer.
Herzwurm (Dirofilaria immitis)
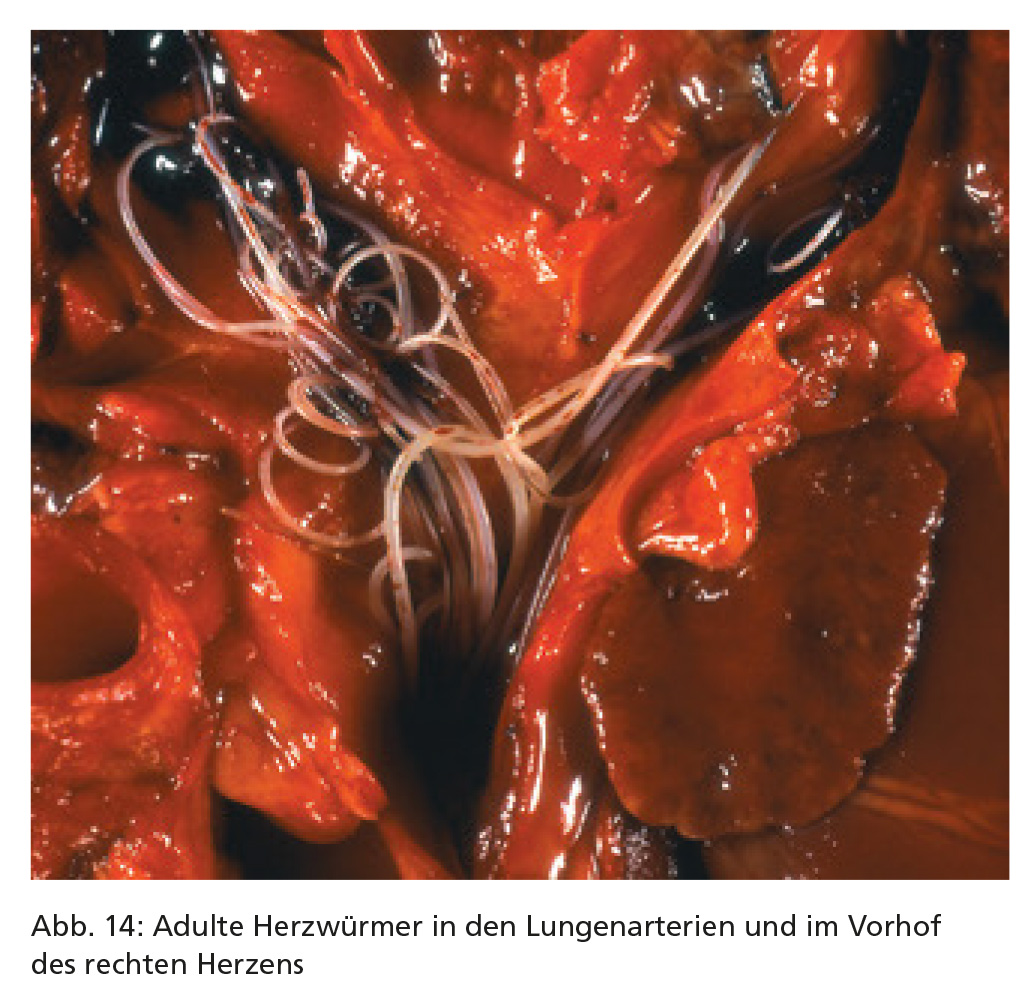
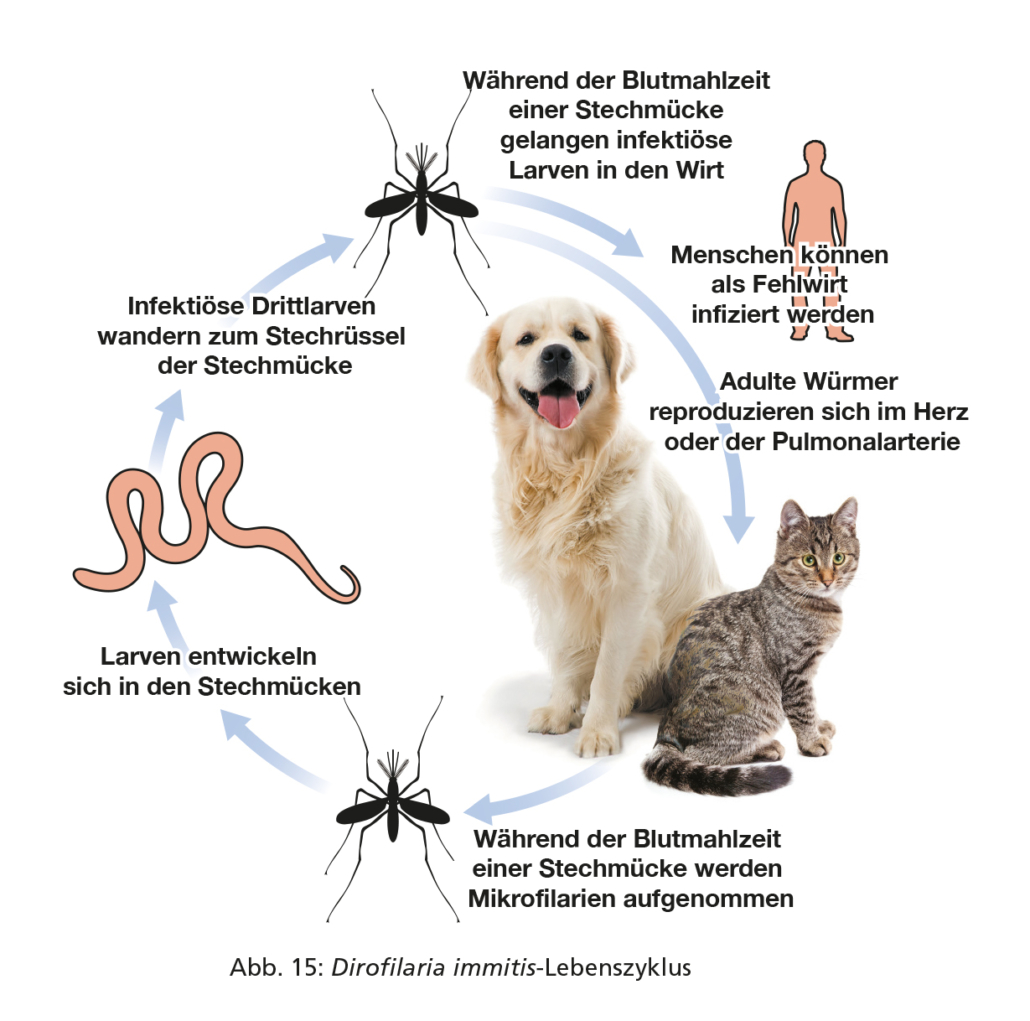
Dirofilaria immitis ist ein bis zu 30 cm langer, nur 1 mm dicker Nematode, der sich in den Lungenarterien und dem Herz von Hunden und Katzen ansiedelt (Abb. 14). Er wird durch Stechmücken übertragen (Abb. 15). Der Herzwurm besitzt ein zoonotisches Potenzial (via Stechmücken), allerdings sind Infektionen bei Menschen sehr selten.
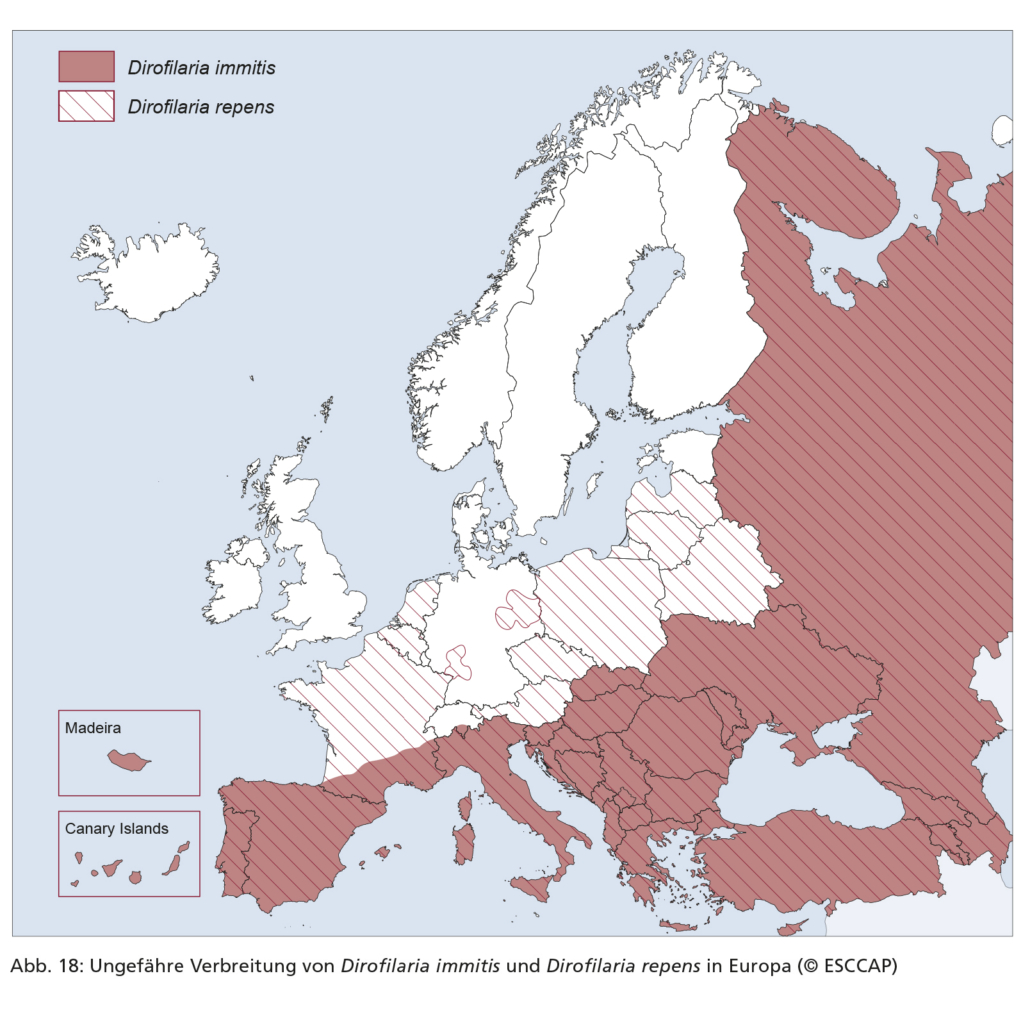
Dirofilaria immitis ist in Südeuropa und zahlreichen Ländern Mittel- und Osteuropas endemisch, allerdings gilt dies gegenwärtig nicht für Deutschland (Abb. 18). In Endemiegebieten ist die Prävalenz bei Hunden etwa zehnmal höher als bei Katzen.
Dirofilaria immitis hat einen indirekten Lebenszyklus. Hunde und Katzen sind Endwirte. Die adulten Parasiten (Makrofilarien) verpaaren sich im Endwirt, die Nachkommen (Mikrofilarien) werden bei der Blutmahlzeit von Stechmücken als Zwischenwirt aufgenommen. In den Stechmücken entwickeln sich die infektiösen Drittlarven, die dann beim nächsten Stechakt auf einen neuen Säugerwirt übertragen werden.
Während der ersten zwei bis vier Monate wandern die Larven durch das Bindegewebe des Säugers, um schließlich über den Blutkreislauf ins Herz oder in die Lungenarterie zu gelangen. Frühestens sechs bis sieben Monate nach der Infektion beginnen die Wurmweibchen (vorausgesetzt, dass sowohl Männchen als auch Weibchen vorhanden sind) mit der Produktion von Mikrofilarien, die ins zirkulierende Blut abgegeben werden (Präpatenz).
Dirofilaria immitis kann potenziell tödliche Erkrankungen bei Hunden und Katzen verursachen. Die Dirofilariose ist eine kardiovaskuläre Erkrankung mit Lungenbeteiligung und eventuell weiteren Organmanifestationen (u. a. Niere). Eine geringe Wurmlast kann symptomlos bleiben. Bei erhöhter Wurmlast und länger bestehender Infektion können unter anderem folgende klinische Anzeichen beobachtet werden: verringerte Belastbarkeit, Schwäche, Atemnot oder chronischer Husten, insbesondere bei erhöhter Belastung.
Wenn die Infektion unbehandelt bleibt, kann sie zu einem Rechtsherzversagen oder Niereninsuffizienz und zum Tod führen. Bei Katzen und Frettchen verläuft die Herzwurminfektion in der Regel ohne Krankheitsanzeichen, führt aber in Einzelfällen u. a. zu respiratorischen Symptomen oder zum plötzlichen Tod. Nähere Details zu klinischen Krankheitsanzeichen werden in der ESCCAP Empfehlung Nr. 5 beschrieben.
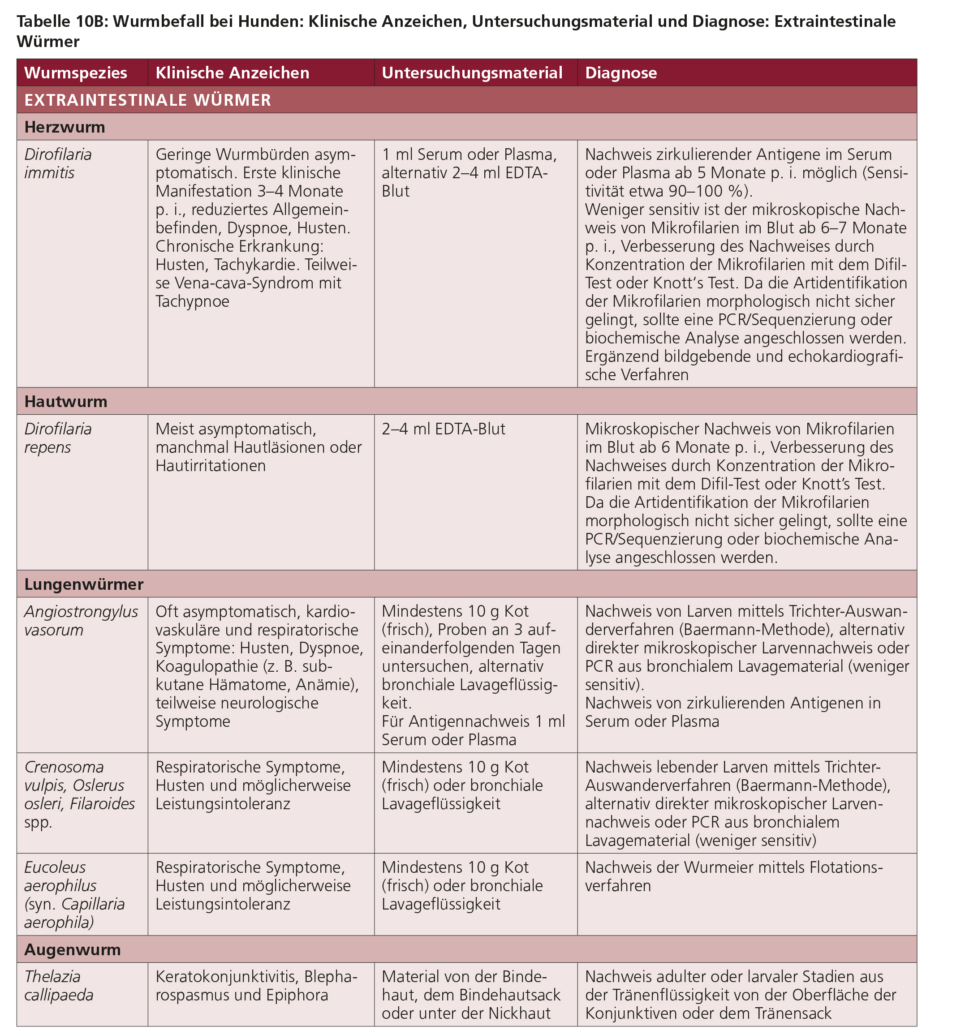
Die Diagnose einer D. immitis-Infektion erfolgt durch den Nachweis zirkulierender Antigene im Serum. Ergänzend können durch mikroskopische Blutuntersuchung Mikrofilarien nachgewiesen werden: Blutproben sollten mittels Knott’s Test oder Filtermethode (s. Guideline Nr. 4, Parasitological diagnosis in Cats, Dogs and Equines) untersucht werden. Diese Methode ist jedoch weniger sensitiv, insbesondere bei Katzen. Bei diesen ist der Nachweis einer D. immitis-Infektion generell schwieriger als beim Hund und sollte neben Labordiagnostik (inkl. Antikörpernachweis) auch Bildgebung des Thorax beinhalten.
Der einzige effektive Wirkstoff, der für die Behandlung gegen adulte Herzwürmer bei Hunden zur Verfügung steht, ist die arsenhaltige organische Verbindung Melarsamin. Die empfohlene Anwendung von Melarsamin ist eine jeweils tief intramuskuläre Injektion des Medikaments (2,5 mg/kg Körpergewicht). Allerdings wird zuvor, d. h. ab einem Monat vor der Melarsamin-Behandlung, eine Behandlung mit Doxycyclin (10 mg/kg Körpergewicht p. o. 2-mal tgl.) empfohlen, um die vorhandenen Herzwürmer durch das Abtöten ihrer Endosymbionten (Wolbachien) zu schwächen. Bei symptomatischen Hunden sollten zusätzlich Glukokortikoide wie Prednisolon verabreicht werden. Falls zirkulierende Mikrofilarien nachgewiesen werden, sollten diese parallel zur Doxycyclin-Behandlung durch zweimalige Behandlung mit einem makrozyklischen Lacton im Abstand von einem Monat eliminiert werden. Zusätzlich sollte unbedingt ein repellierendes Insektizid angewendet werden, um eine Übertragung bzw. Ausbreitung des Parasiten zu verhindern. Nach 30–60 Tagen folgt eine zweite und einen Tag später eine dritte Injektions-Behandlung. Möglichen Komplikationen aufgrund pulmonaler Thromboembolien sollte durch die Gabe von Heparin und eines Kortikosteroids (z. B. Prednisolon 0,5 mg/kg BID 1. Woche, 0,5 mg/kg SID 2. Woche, 0,5 mg/kg EOD 3. und 4. Woche) vorgebeugt werden. Zudem sollte zwingend eine strikte Bewegungsrestriktion während der gesamten Behandlungs- und Erholungsdauer unbedingt bis zum Ende des Therapieschemas (Tag 91) erfolgen. Anschließend kann die strikte Käfigruhe beendet werden, weitere Bewegungsrestriktionen (Leinenzwang) sollten aber noch für 6–8 weitere Wochen beibehalten werden.
CAVE: Die hier beschriebene Therapie gilt nur für den Hund, u. a. da bei D. immitis-infizierten Katzen häufig eine Spontanheilung nach 18–48 Monaten eintritt. Währenddessen sollte eine Prednisolon-Behandlung (2 mg/kg Körpergewicht EOD) durchgeführt werden. Zudem besteht bei Anwendung von Melarsamin bei der Katze ein hohes Risiko für Thromboembolien und anaphylaktische Reaktionen. Bei Katzen mit schweren Anzeichen von Herzwurm-assoziierten Atemwegserkrankungen wird eine Behandlung mit einer hohen Prednisolon-Dosis (1–2 mg/kg Körpergewicht 3-mal pro Tag) empfohlen.
Die Vermeidung der Herzwurmerkrankung bei Hunden und Katzen in Endemiegebieten hängt maßgeblich von einer vorbeugenden Behandlung ab. Hierbei werden nach erfolgter Infektion die larvalen Herzwurmstadien abgetötet, bevor sie das Herz bzw. die Lungenarterie erreicht haben. Dies wird durch den monatlichen Einsatz von makrozyklischen Lactonen (topisch oder oral) während der Übertragungssaison (üblicherweise von April bis November) erreicht. Da die makrozyklischen Lactone lediglich gegen die frühen Larvenstadien während der ersten vier Wochen post infectionem wirksam sind, ist bei längerem Aufenthalt in Endemiegebieten eine monatliche Behandlung unbedingt erforderlich. Bei Reisen in Endemiegebiete, die kürzer als vier Wochen dauern, muss eine Behandlung unmittelbar nach der Rückreise erfolgen. Bei länger dauernden Reisen ist monatlich und ebenfalls einmal direkt nach der Rückkehr zu behandeln.
In Europa sind vorbeugende Behandlungen gegen D. immitis-Larven aktuell voll wirksam, allerdings zeigen Untersuchungen aus den USA, dass dort Herzwurmpopulationen mit Resistenzen gegen makrozyklische Lactone existieren. Um die für die Aufrechterhaltung der Tiergesundheit essenzielle Wirksamkeit der makrozyklischen Lactone aufrechtzuerhalten bzw. das Risiko einer Resistenzentwicklung zu senken, wird in endemischen Regionen u. a. die Anwendung von die Blutsaugeraktivität der Stechmücken verhindernden Mitteln (Repellentien) empfohlen.
Ausführliche Informationen zur Herzwurminfektion bei Hunden und Katzen finden Sie in der ESCCAP-Empfehlung Nr. 5: Bekämpfung von vektorübertragenen Krankheiten bei Hunden und Katzen sowie auf der Internetseite der Amerikanischen Herzwurmgesellschaft sowie der Society of Dirofilariosis and Angiostrongylosis.
Hautwurm (Dirofilaria repens)
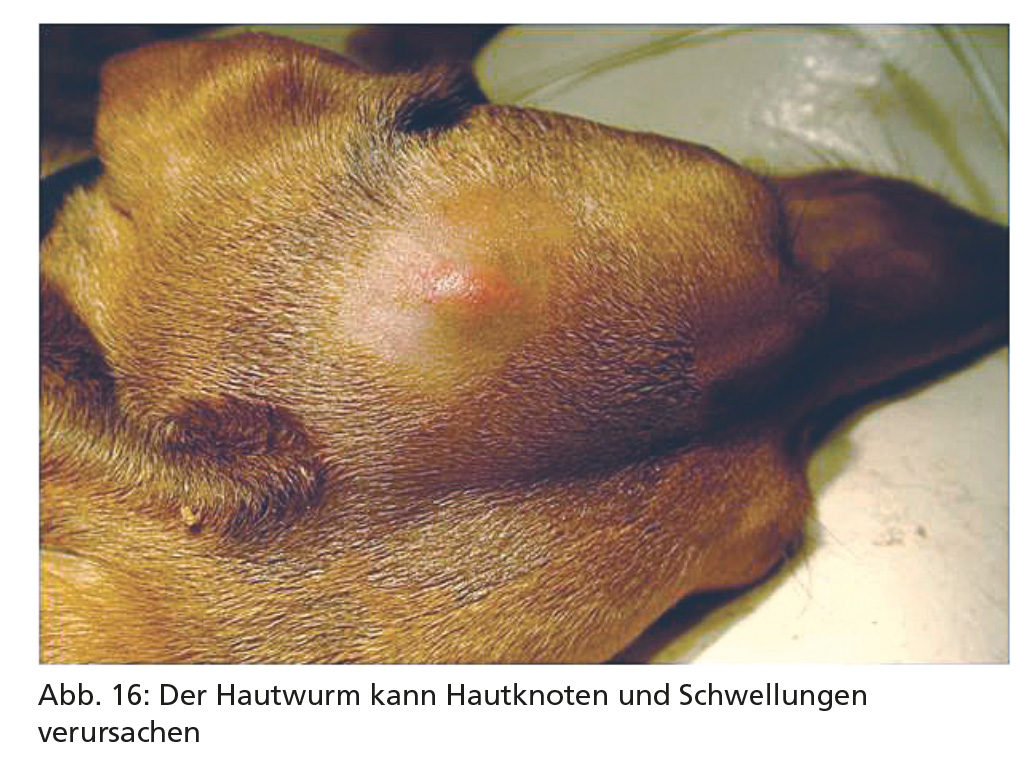
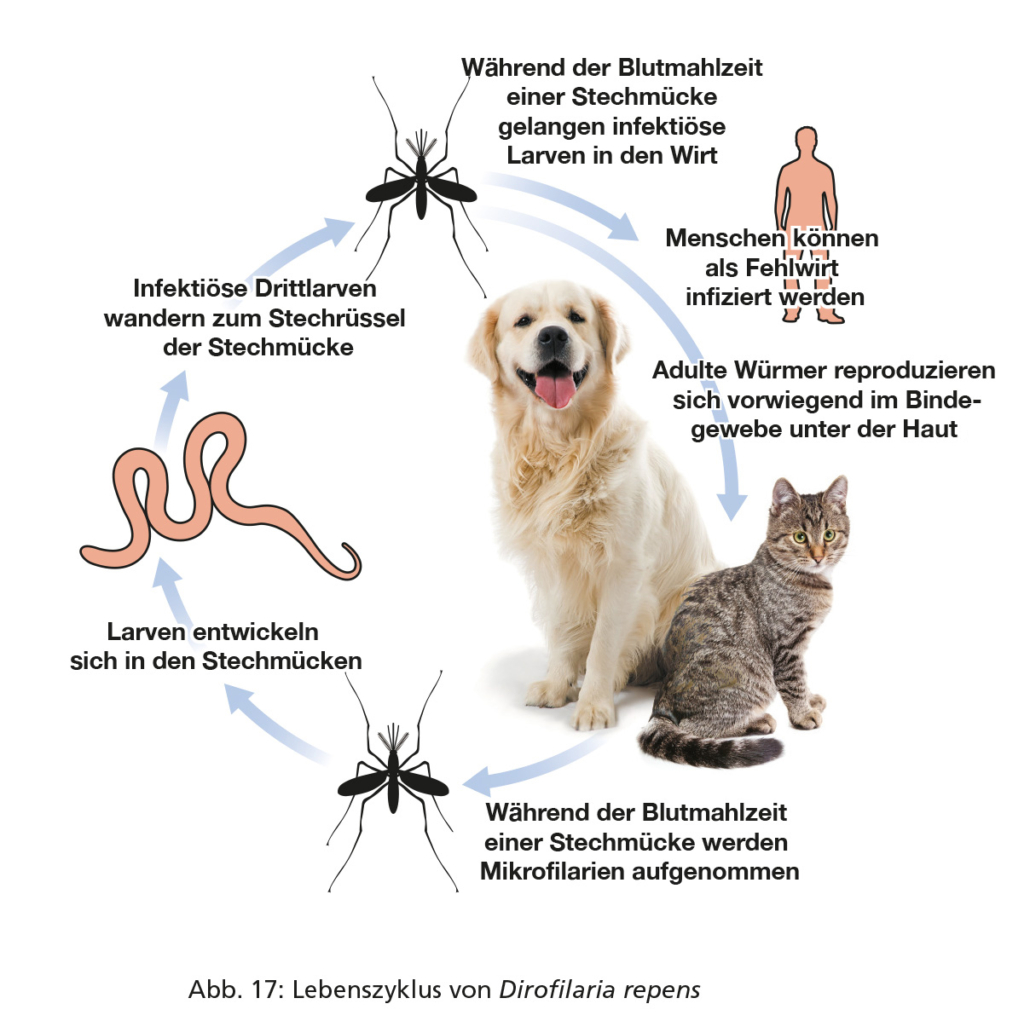
Dirofilaria repens ist ein bis zu 17 cm langer Nematode, dessen adulte Stadien (Makrofilarien) im Unterhautgewebe von Hunden und Katzen vorkommen (Abb. 16). Die Übertragung findet über Stechmücken (Abb. 17) als Zwischenwirte statt. Der Hautwurm ist die wichtigste zoonotische Filarienart in Europa.
In vielen Regionen Europas überschneiden sich die Endemiegebiete von D. repens und D. immitis. Dabei ist D. repens in vielen Regionen der häufigere Erreger, z. B. in Nordfrankreich und Ungarn. Das Verbreitungsgebiet von D. repens (s. Abbildung 18) weitet sich in Europa aus und hat fokal auch Deutschland, Österreich, die Niederlande, Polen und Litauen erreicht (s. Abbildung 18).
Wurmweibchen gebären Mikrofilarien, die im Blutkreislauf über viele Monate zirkulieren. Sie werden von Stechmücken bei der Blutmahlzeit aufgenommen, wo die Entwicklung zu infektiösen Drittlarven stattfindet, die beim folgenden Stechakt wieder auf Säuger übertragen werden und danach im subkutanen Bindegewebe zu adulten Würmern heranreifen und wiederum Mikrofilarien produzieren. Die erwachsenen Würmer befinden sich zwischen den subkutanen und tiefen Bindegewebsschichten in den meisten Körperorganen. Adulte Würmer können mehrere Jahre alt werden.
Dirofilaria repens ist der häufigste Erreger der subkutanen Filariose bei Hunden und Katzen in Mitteleuropa, die in Gebieten wie Nordfrankreich und Ungarn endemisch ist. Die meisten Infektionen verlaufen asymptomatisch, in manchen Fällen bilden sich im subkutanen Bindegewebe oder in den Konjunktiven schmerzlose verschiebbare Knoten, die Wurmstadien enthalten. Bei einer massiven Infektion kann es zu einer schweren Dermatitis kommen. Vereinzelt werden durch D. repens Knoten in der Lunge verursacht, oder es kommt zur Ansiedlung von Wurmstadien in den Körperhöhlen (diese werden gelegentlich bei Kastrationen gefunden).
Mikrofilarien von D. repens können bei Hunden durch mikroskopische Blutuntersuchungen nachgewiesen werden; Hinweise zu weiteren diagnostischen Details finden sich in der ESCCAP-Empfehlung Nr. 4. Bei Katzen lassen sich die Mikrofilarien nur schwer nachweisen, da die Mikrofilariendichte im Blut sehr gering ist oder gar keine Mikrofilarien produziert werden.
Ein Befall mit larvalen und adulten D. repens-Stadien sollte mit einem hierfür zugelassenen makrozyklischen Lacton behandelt werden. Adulte Würmer können durch sechs im monatlichen Abstand erfolgende Moxidectin-Behandlungen eliminiert werden. Knoten, beispielsweise in den Konjunktiven, werden chirurgisch oder besser (weil weniger invasiv) mittels Aspiration per Katheter entfernt. Aufgrund des zoonotischen Potenzials sollten Hunde in Endemiegebieten während der Übertragungssaison (üblicherweise von April bis November) monatlich mit einem makrozyklischen Lacton behandelt werden. Bei nachgewiesener Mikrofilarämie sollte zusätzlich zu einer monatlichen Behandlung mit einem makrozyklischen Lacton unbedingt ein repellierendes Insektizid angewendet werden, um eine weitere Ausbreitung des Parasiten bzw. eine Endemisierung in bisher nicht endemischen Regionen zu verhindern.
Vor einer patenten Hautwurm-Infektion schützt die monatliche Behandlung mit einem makrozyklischen Lacton während der Übertragungssaison (üblicherweise von April bis November). Bei Reisen in Endemiegebiete, die kürzer als vier Wochen dauern, sollte eine Behandlung unmittelbar nach der Rückreise erfolgen. Bei länger dauernden Reisen ist monatlich und zusätzlich einmal direkt nach der Rückkehr zu behandeln (s. a. Angaben zu D. immitis). Wenn ein Tier aus einem Endemiegebiet in ein Nichtendemiegebiet verbracht werden soll, ist es angezeigt, sein Blut auf Mikrofilarien zu untersuchen. Im positiven Fall sollte noch im Endemiegebiet und spätestens 30 Tage nach Ankunft im Nichtendemiegebiet eine Behandlung gegen Mikrofilarien erfolgen und ein repellierendes Insektizid angewendet werden
Zoonosepotenzial von D. immitis und D. repens
In Europa ist D. repens der bedeutendste Erreger von Filarieninfektionen des Menschen. Als häufigste Befunde gelten subkutane Knoten oder Knoten unter der Konjunktiva des Auges, in denen sich dann die adulten Würmer befinden. Es kommt jedoch auch zur Ansiedlung in verschiedenen inneren Organen (meistens Lunge) und dortiger Granulombildung. Dies bleibt in der Regel klinisch inapparent. Trotzdem ist aufgrund des zoonotischen Potenzials von D. repens eine Bekämpfung dieser Parasitose bei Hunden und Katzen sehr wichtig. Mikrofilarämische Hunde und Katzen sollten monatlich mit makrozyklischen Lactonen behandelt werden, zusätzlich sollte unbedingt ein repellierendes Insektizid angewendet werden.
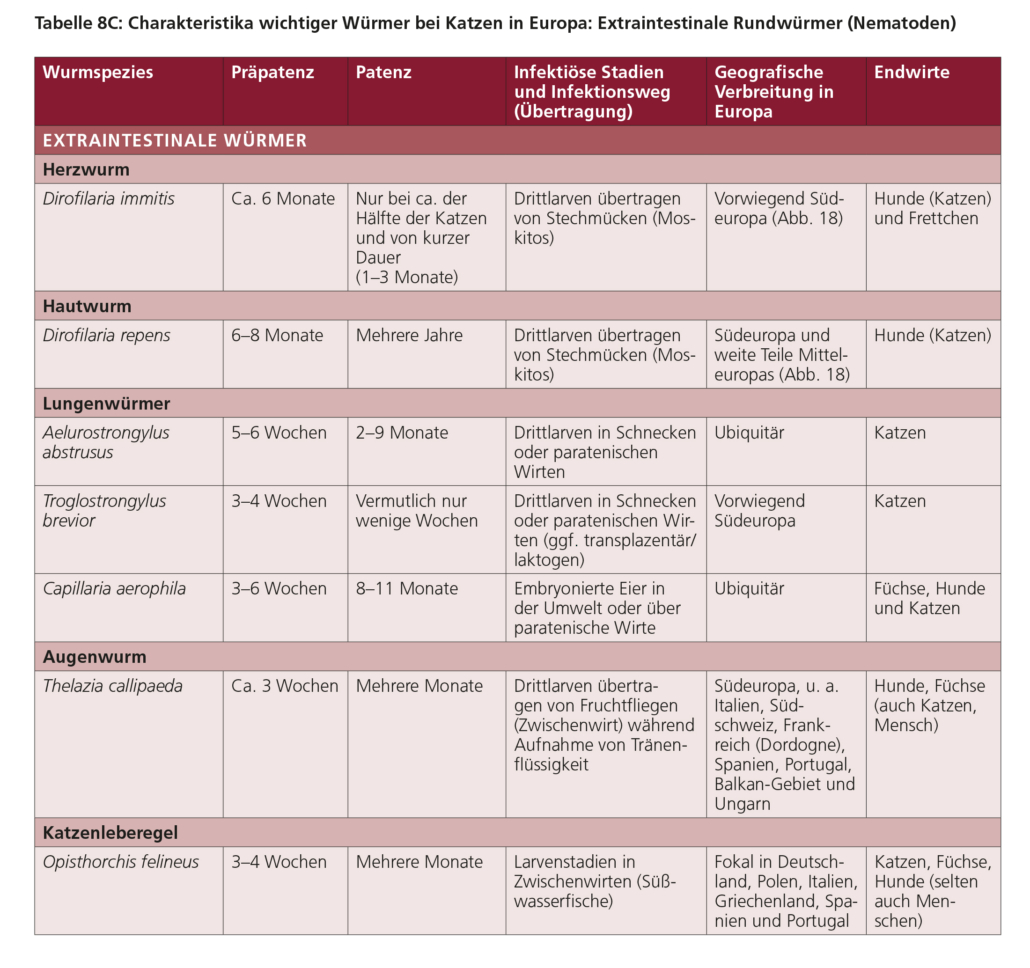
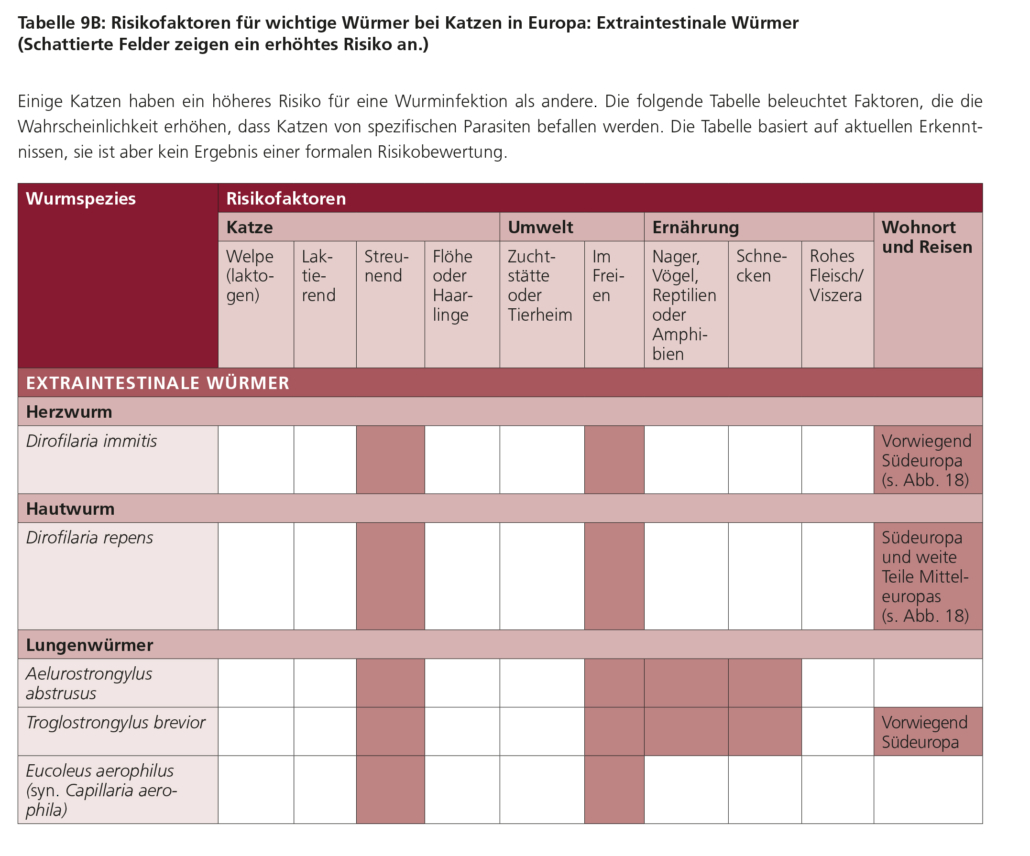
Weitere Informationen zu den Charakteristika von Dirofilaria spp., Risikofaktoren, klinischen Anzeichen, Diagnose und Behandlung finden Sie in den Tabellen 6C, 7, 8C und 9–11 sowie in der ESCCAP-Empfehlung Nr. 5: Bekämpfung von vektorübertragenen Krankheiten bei Hunden und Katzen unter www.esccap.de.
5.4. Lungenwürmer (Angiostrongylus vasorum, Crenosoma vulpis, Aelurostrongylus abstrusus)
Angiostrongylus vasorum ist ein Nematode, dessen adulte Stadien die Lungenarterie und rechte Herzkammer von Hunden sowie anderen Caniden (Endwirte) besiedeln. Dieser Parasit kommt in Deutschland und der Mehrzahl der europäischen Länder vor. Als Reservoirwirte dienen vor allem Rotfüchse, aber auch andere Wildcaniden. Der Parasit wird bis zu 18 mm lang, und die Männchen besitzen eine kleine Bursa copulatrix, während die Weibchen einen blutgefüllten Darm haben, um den sich der Uterus windet.
Etwas seltener kommt bei Hunden ein Befall mit Crenosoma vulpis vor, der als adulter Wurm die Bronchien und Trachea besiedelt. Auch C. vulpis kommt in vielen europäischen Ländern inklusive Deutschlands vor, und insbesondere Rotfüchse dienen neben anderen Wildcaniden als Reservoirwirte. Adulte C. vulpis sind 4–15 mm lang und durch ein charakteristisches Hinterende gekennzeichnet, welches eine Cuticula mit ca. 20 überlappenden Falten (Schachtelhalm-artig) mit kleinen Dornen aufweist.
Der bei der Katze vorkommende Lungenwurm Aelurostrongylus abstrusus besiedelt als adulter Wurm die Bronchiolen und Alveolen. Eine Infektion mit A. abstrusus wurde in Deutschland und der Schweiz bei ca. 10–16 % der untersuchten Hauskatzen nachgewiesen. Bei Wildkatzen in Rheinland-Pfalz wurde in einer kürzlich veröffentlichten Studie Angiostrongylus chabaudi als häufigster (53 %), A. abstrusus mit 42 % und als weiterer Lungenwurm Troglostrongylus brevior bei 31 % der insgesamt 128 untersuchten Tiere nachgewiesen. Aelurostrongylus abstrusus wird bis zu 10 mm lang und ist sehr dünn (weniger als 100 µm).
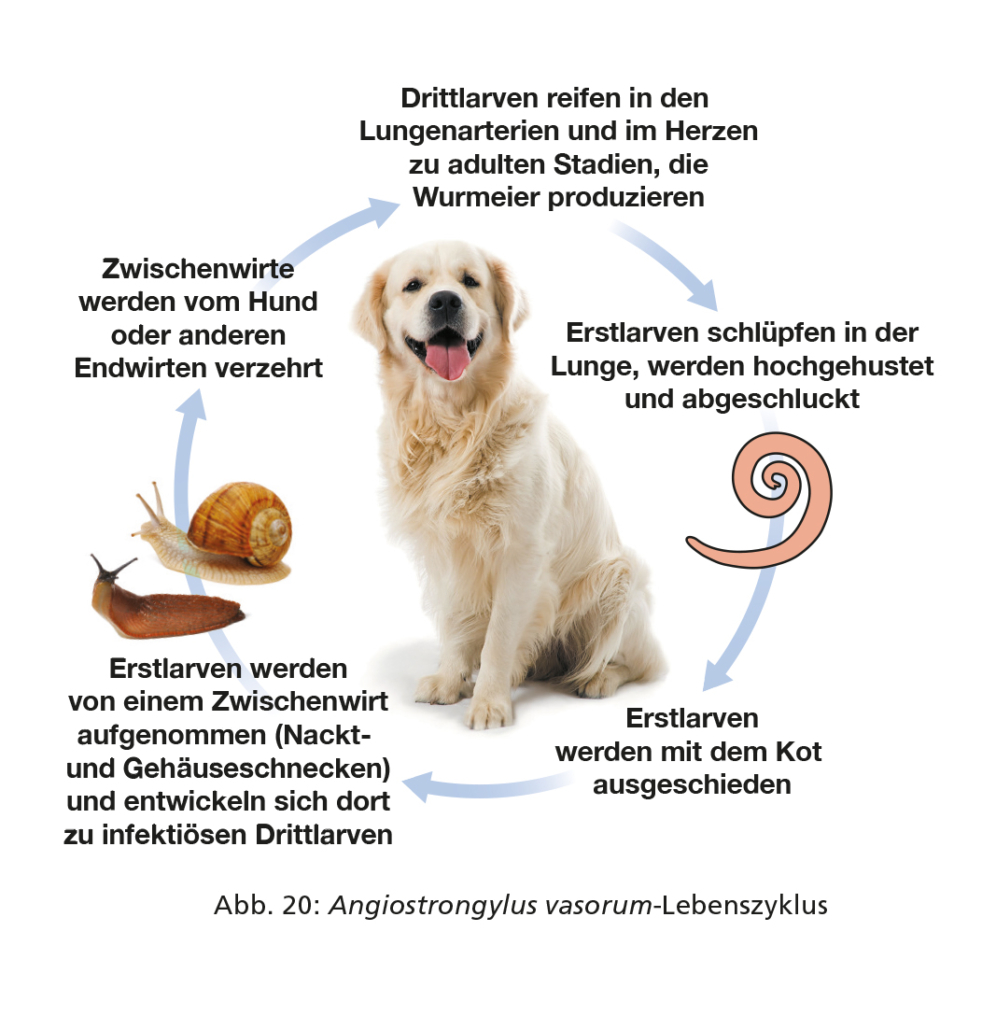
Lungenwurm-infizierte Endwirte scheiden mit dem Kot Erstlarven aus. Diese werden von Nackt- und Gehäuseschnecken als Zwischenwirte aufgenommen und entwickeln sich dort zu infektiösen Drittlarven; experimentell erwiesen sich zudem Grasfrösche oder andere Schnecken-verzehrende Tiere als paratenische oder Zwischenwirte. Endwirte infizieren sich durch Verzehr von paratenischen oder Zwischenwirten. Als weiterer Infektionsweg ist die direkte orale Aufnahme von durch Schnecken in die Umwelt freigesetzten Drittlarven (z. B. durch das Fressen von Gras) zu berücksichtigen. So zeigte eine kürzlich vorgenommene experimentelle Studie, dass Drittlarven von A. vasorum und C. vulpis nach der Ausscheidung durch die Zwischenwirtsschnecken für mindestens 8 Wochen infektiös bleiben.
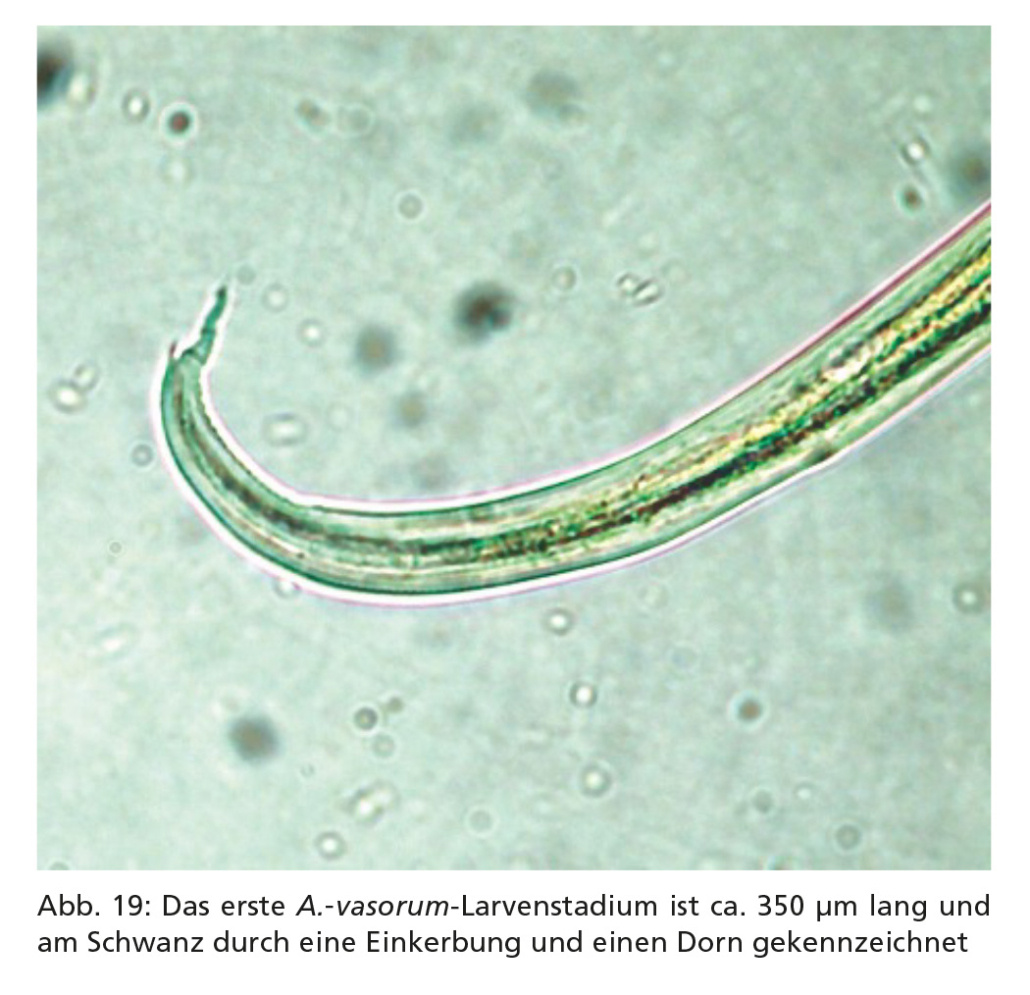
Nach Aufnahme durch den Endwirt wandern die Larven zum rechten Herz und der Lungenarterie (A. vasorum) bzw. weiter zur Lunge bzw. den luftführenden Wegen (C. vulpis, A. abstrusus) und reifen dort zu Adultstadien heran. Die Produktion larvenhaltiger Eier beginnt bei weiblichen A. vasorum-Würmern 6–8 Wochen, bei C. vulpis 3 Wochen und bei A. abstrusus 5–6 Wochen nach der Infektion. Die rasch aus den Eiern schlüpfenden Larven werden retrograd über das tracheale Flimmerepithel in die Maulhöhle transportiert bzw. hochgehustet, dann abgeschluckt und mit dem Kot ausgeschieden (s. Abb. 20, 21). Ohne anthelminthische Behandlung können adulte A. vasorum-Würmer möglicherweise lebenslang in ihrem Endwirt persistieren.
Die klinischen Manifestationen einer A. vasorum-Infektion bei Hunden sind unterschiedlich. Die Infektion kann ohne klinische Anzeichen verlaufen, häufig kommt es jedoch zu respiratorischen Symptomen (Husten, Dyspnoe) infolge einer verminösen Pneumonie. Mögliche weitere Erscheinungen sind Blutgerinnungsstörungen, neurologische, gastrointestinale oder unspezifische Symptome wie Anorexie und Leistungsabfall. Bei chronischer Infektion können Anorexie, Gewichtsverlust, Kachexie, Anämie und pulmonale Hypertonie sowie Zeichen einer Blutgerinnungsstörung (z. B. subkutane Einblutungen, Nasenbluten, Hämoptyse, Melena oder verlängertes Bluten bei Wunden) auftreten. In seltenen Fällen kommt es zu plötzlichen Todesfällen. Gelegentlich befinden sich Larven und selten auch adulte Stadien von A. vasorum in ektopischen Lokalisationen wie Gehirn, Harnblase, Niere oder vorderer Augenkammer. Die Symptome entsprechen den Schädigungen in den befallenen Organen. Teilweise kommt es zu Todesfällen.
Mit C. vulpis infizierte Hunde zeigen eine katarrhalische Bronchitis mit Eosinophilie bis hin zu einer Bronchopneumonie. Die häufigsten klinischen Anzeichen sind Husten, Tachypnoe, Dyspnoe und Niesen sowie unspezifische Merkmale wie Fieber und eine schlechte Konstitution.
Bei Katzen mit einer A. abstrusus-Infektion bilden sich um die in den Alveolen und Bronchiolen vorhandenen Würmer bis zu 10 mm große, meist subpleural liegende Knötchen. Infektionen mit geringen A. abstrusus-Wurmbürden verlaufen meist ohne Krankheitserscheinungen, während Katzen mit starkem Befall Husten, Niesen, Nasenausfluss, erhöhte Atemfrequenz sowie Sauerstoffunterversorgung und Kümmern aufweisen können. Unbehandelt kann die Infektion tödlich verlaufen.
Lungenwurmlarven sind mittels Trichter-Auswanderverfahren nach Baermann im Frischkot (> 10 g) nachweisbar. Dabei empfiehlt es sich, den Kot so frisch wie möglich zu untersuchen. Da die tägliche Larvenausscheidung stark schwanken kann, sollte im Verdachtsfall bei negativem Nachweis die Untersuchung an ein oder zwei aufeinanderfolgenden Tagen wiederholt werden. Die Larven (oder deren DNA mittels PCR) können auch in der Spülflüssigkeit einer Bronchiallavage gefunden werden, die Untersuchung des Lavagematerials ist jedoch weniger sensitiv. Bei starkem A. vasorum-Befall kann sogar der Larvennachweis in einem rektalen Kotabstrich gelingen. Für diesen Parasiten sind außerdem kommerzielle Tests erhältlich, mit denen im Serum zirkulierendes A. vasorum-Antigen nachweisbar ist. Bei Verdacht auf entzündliche Prozesse in der Lunge sollten bildgebende Verfahren (Röntgen, Computertomografie) angewandt werden, um möglicherweise vorhandene interstitielle und peribronchiale Veränderungen zu erkennen.
Zur Behandlung eines A. vasorum– oder C. vulpis-Befalls werden makrozyklische Lactone verwendet. Zu beachten ist, dass bei manchen zugelassenen Präparaten wiederholte Behandlungen gegen A. vasorum notwendig sind. Bei hochgradigen Symptomen sind neben einer Infusionstherapie fallspezifisch weitere unterstützende Maßnahmen notwendig (z. B. Antiinfektiva, Bluttransfusionen, Glukokortikoide, O2-Therapie), inklusive Maßnahmen zur Verhinderung der Blutungsneigung. Zudem sollte der Hund während der Therapie ruhig gehalten werden (mind. 2–3 Tage).
Zur Therapie von A. abstrusus-Infektionen sind sowohl makrozyklische Lacton- also auch Emodepsid-haltige Präparate zugelassen, die teilweise wiederholt anzuwenden sind. Durch die regelmäßige prophylaktische Gabe eines wirksamen Anthelminthikums kann einer Erkrankung zuverlässig vorgebeugt werden. Wenn möglich, sollten Hunde und Katzen grundsätzlich davon abgehalten werden, Schnecken zu verzehren.
Weitere Informationen über die Eigenschaften von A. vasorum, Risikofaktoren, klinische Anzeichen, Diagnose und Behandlungen finden Sie in den Tabellen 6C, 7, 8C und 9–11 sowie in der ESCCAP-Empfehlung Nr. 4 Parasitological Diagnosis in Cats, Dogs and Equines.
5.5. Hakenwürmer
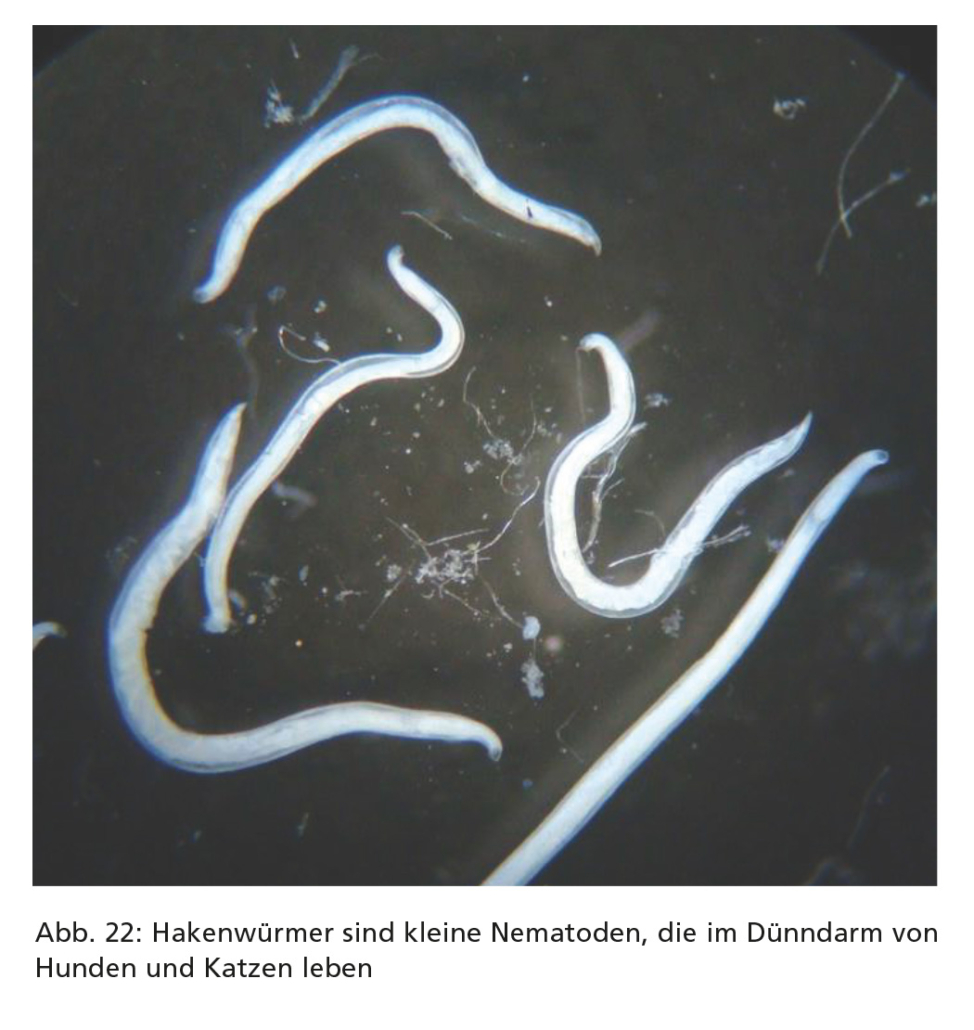
Hakenwürmer sind ca. 0,5–1,5 cm große Nematoden, die als adulte Stadien im Dünndarm leben (Abb. 22). Sie können schwer verlaufende Erkrankungen bei Hunden und Katzen auslösen.
Einige Arten sind Zoonoseerreger. Die geläufige Bezeichnung „Hakenwürmer“ leitet sich von ihrem hakenförmig gebogenen Vorderende ab. Um sich zu ernähren, heften sich alle Spezies mit ihrer großen Mundöffnung an die Darmschleimhaut und verletzen dabei deren Oberfläche. Betroffen sind häufig Hunde, die zu mehreren in Zwingern oder Ausläufen gehalten werden.
In Europa gibt es drei Hakenwurmarten: Uncinaria stenocephala parasitiert bei Hunden und selten bei Katzen, Ancylostoma tubaeforme nur bei Katzen. Beide genannten Hakenwurmarten kommen in allen europäischen Regionen vor. Ancylostoma caninum ist nur bei Hunden und fast ausschließlich in den wärmeren Regionen Südeuropas zu finden.
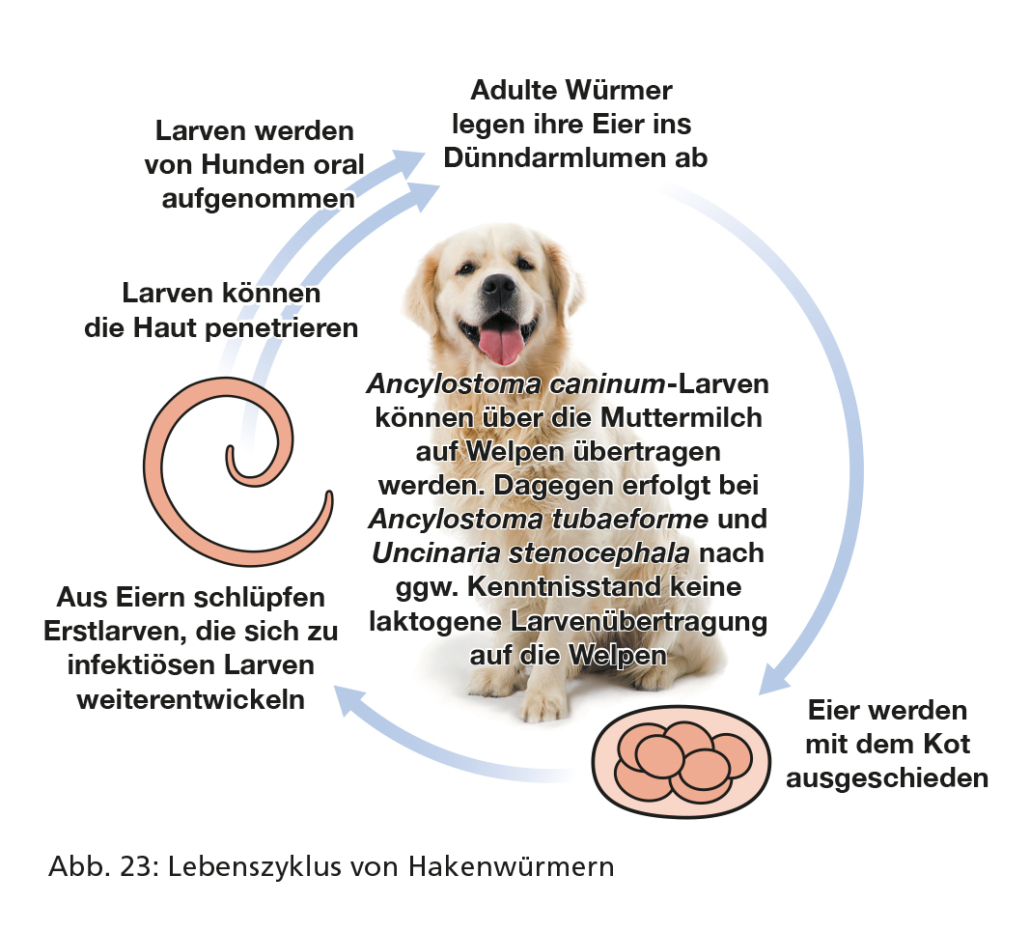
Im Dünndarm produzieren Hakenwurmweibchen Eier, die mit dem Kot ausgeschieden werden (Abb. 23). In der Außenwelt entwickelt sich in der Eihülle eine erste Larve, die sich nach dem Schlupf binnen einiger Tage zum infektiösen dritten Larvenstadium weiterentwickelt. Diese Larven können aktiv durch die Haut eines Wirts eindringen oder werden oral aufgenommen. Sie entwickeln sich, bei Ancylostoma-Arten unter Einbezug einer Körperwanderung, innerhalb von zwei bis vier Wochen nach der Infektion im Dünndarm zu adulten Würmern.
Ancylostoma spp.-Larven gelangen oft durch Penetration der Haut in den Wirt. Es wird angenommen, dass dieser Infektionsweg für U. stenocephala epidemiologisch von untergeordneter Bedeutung ist und stattdessen der orale Infektionsweg vorherrscht. Durch die laktogene Übertragung können sich säugende Hundewelpen mit A. caninum-Larven infizieren. Dagegen gibt es bei A. tubaeforme und U. stenocephala keine Larvenübertragung mit der Muttermilch. Bis zur Eiausscheidung dauert es bei infizierten Welpen bzw. Kitten ca. zwei, bei älteren Tieren eher drei bis vier Wochen. Bei Ancylostoma-Arten kann es auch zur Infektion über die Aufnahme von infizierten paratenischen Wirten (z. B. Nagern) kommen.
Typische Symptome eines starken Hakenwurmbefalls sind Durchfall und Gewichtsverlust. Aufgrund ihrer hämatophagen Ernährungsweise können bei Infektionen mit Ancylostoma-Arten zudem Anämie und okkultes Blut im Durchfallkot auftreten. Die Übertragung von A. caninum-Larven über die Muttermilch kann eine akute Anämie verursachen, die für Welpen tödlich enden kann. Bisweilen treten an den Pfoten bei Hund oder Katze Hautentzündungen auf, die Folgen der perkutanen Einwanderung der Hakenwurmlarven sind. Bei Menschen kann die perkutane Infektion mit Hakenwurmlarven (v. a. A. caninum) zum Krankheitsbild der Larva migrans cutanea führen.
Die Diagnose eines Hakenwurmbefalls basiert auf dem koproskopischen Nachweis der Eier mittels der Flotationsmethode. Es ist allerdings nicht zuverlässig möglich, die Eier der verschiedenen Hakenwurmarten mikroskopisch zu differenzieren (Abb. 24). Außerdem ist ein auf dem Nachweis von Hakenwurm-Antigen basierender Kopro-Antigen-ELISA verfügbar und gewöhnlich bereits vor dem Beginn der Eiausscheidung positiv. Bei Hundewelpen, die mit A. caninum laktogen infiziert wurden, können Krankheitszeichen noch vor Beginn der Eiausscheidung auftreten (allerdings kann der Kopro-Antigen-Test bereits positiv sein).
Mit Hakenwürmern infizierte Hunde und Katzen sind mit einem wirksamen Anthelminthikum zu behandeln. Dabei ist auf eine ausreichende Wirkung auf die festgestellte Hakenwurmart zu achten, da deutliche Wirksamkeitsunterschiede für die verschiedenen Wirkstoffe bestehen können. Wenn Jungtiere eine Infektion aufweisen, kann zusätzlich zur anthelminthischen Behandlung eine unterstützende Therapie erforderlich sein. Nach einer überstandenen Infektion bildet sich eine Immunität aus, diese ist allerdings nicht immer vollständig schützend. Daher sollten Tiere, die einem hohen Reinfektionsdruck ausgesetzt sind (z. B. Welpen und Jungtiere in Zuchten), regelmäßig entwurmt werden. Zudem sollte die Umgebung dekontaminiert und die Tiere währenddessen woanders untergebracht werden. Bei Hunden und Katzen in Gruppenhaltung, beispielsweise in Zwingern und Ausläufen mit Naturboden, ist eine regelmäßige tierärztliche Beobachtung notwendig.
Weitere Informationen zu den Charakteristika der Hakenwürmer, Risikofaktoren, klinischen Anzeichen, Diagnose und Behandlungen finden Sie in den Tabellen 6B, 7, 8B und 9–11 sowie in der ESCCAP-Empfehlung Nr. 4 Parasitological Diagnosis in Cats, Dogs and Equines.
5.6. Peitschenwürmer (Trichuris vulpis)
Trichuris vulpis ist ein bis zu 8 cm langer Dickdarmnematode mit langem, dünnem Vorder- und kurzem, dickem Hinterteil. Er kann bei Hunden und anderen Caniden zu Erkrankungen führen. Trichuris vulpis kommt vor allem in Teilen Zentral- und Südeuropas und unter speziellen Haltungsbedingungen wie bei Gruppenhaltung in Zwingern oder Tierheimen vor. Die Umwelt kann in beträchtlichem Maße und persistent mit infektiösen Eiern kontaminiert sein. Eine solche Kontamination kann anhaltende Probleme bereiten, da sich Hunde in einer kontaminierten Umgebung wiederholt reinfizieren können.
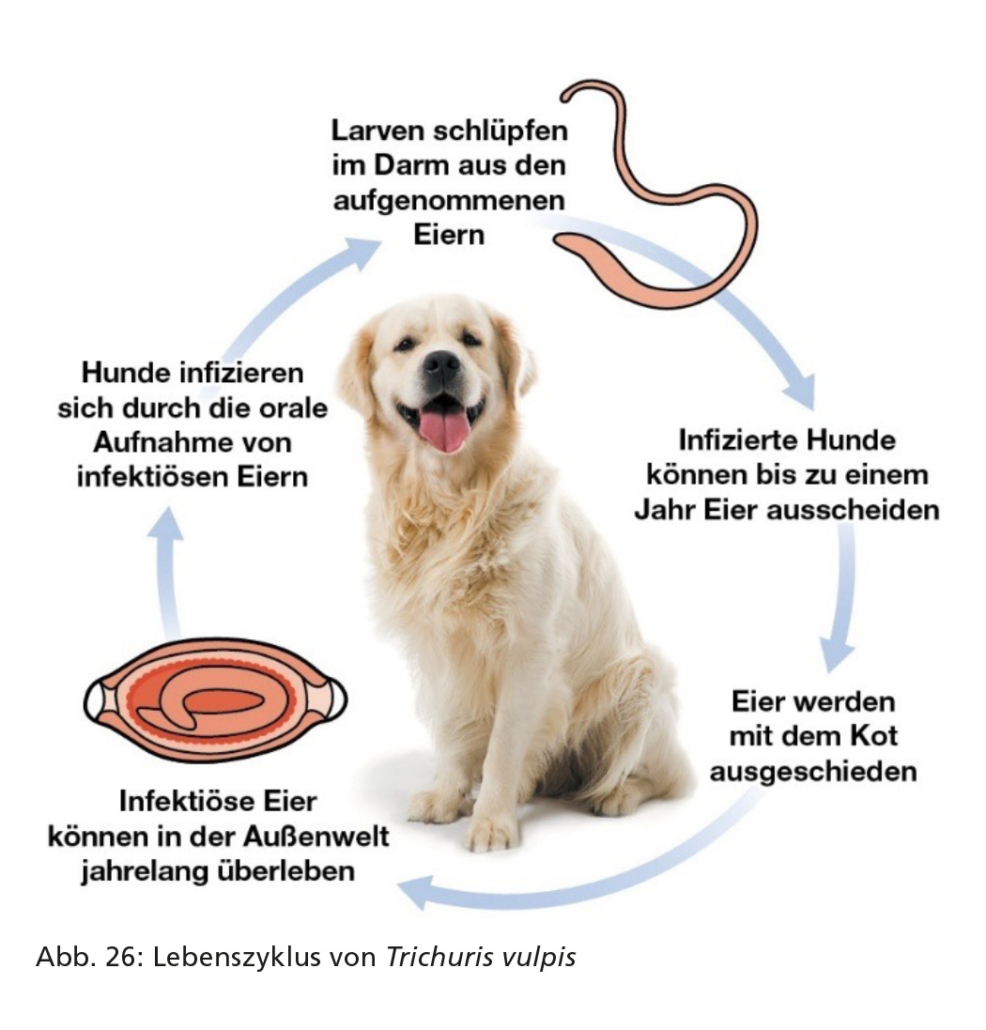
Infizierte Hunde scheiden Trichuris-Eier mit dem Kot aus. Bei Temperaturen über +4 °C entwickelt sich im Ei innerhalb von ein bis zwei Monaten, bei 25 °C in ca. fünf Wochen das erste Larvenstadium (L1), das infektiös für Caniden ist. Die Larven sind durch die Eischale geschützt und können in der Umwelt mehrere Jahre infektiös bleiben. Hunde infizieren sich durch die orale Aufnahme von Eiern, die infektiöse Larven enthalten (Abb. 25). Die Würmer sind mit ihrem dünnen Vorderende in der Dickdarmschleimhaut verankert, wo sie sich von Gewebe und Blut ernähren. Die Präpatenz beträgt neun bis zehn Wochen, wonach über einen Zeitraum von bis zu über einem Jahr Eier ausgeschieden werden können.
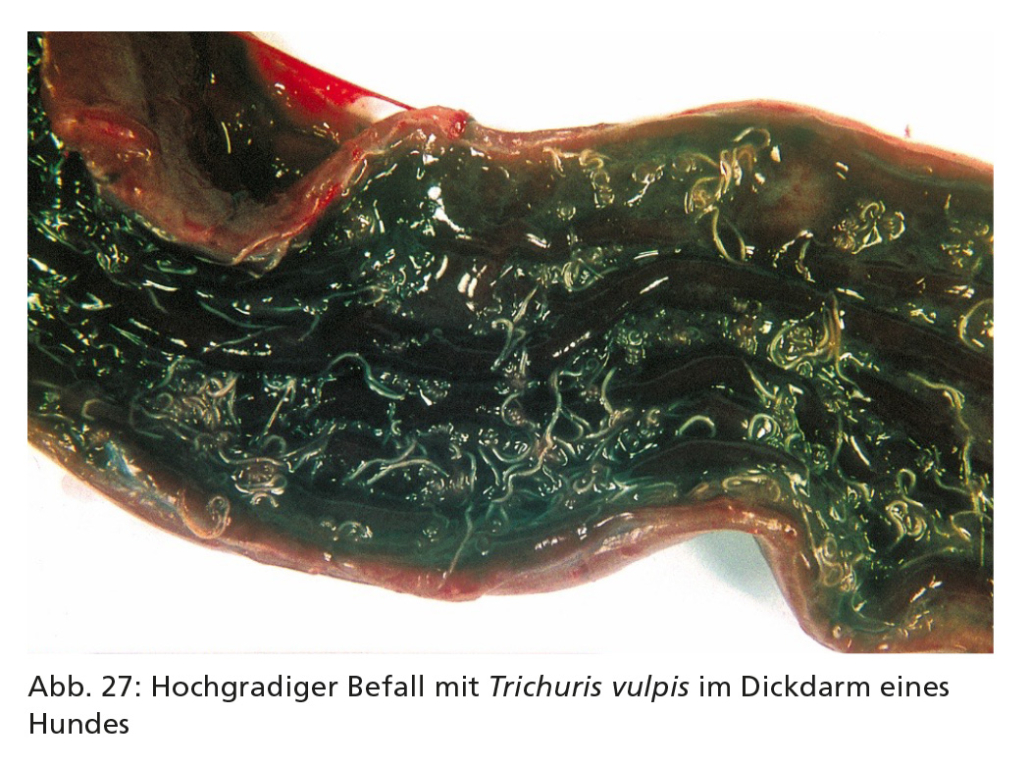
Hochgradiger Peitschenwurmbefall (Abb. 27) verursacht eine Dickdarmentzündung mit blutigem, schleimigem Kot oder Durchfall; auch können Gewichtsverlust, Anämie und Elektrolytimbalanzen einschließlich Hyponatriämie (auch als Pseudo-Addison-Erkrankung bezeichnet) auftreten.
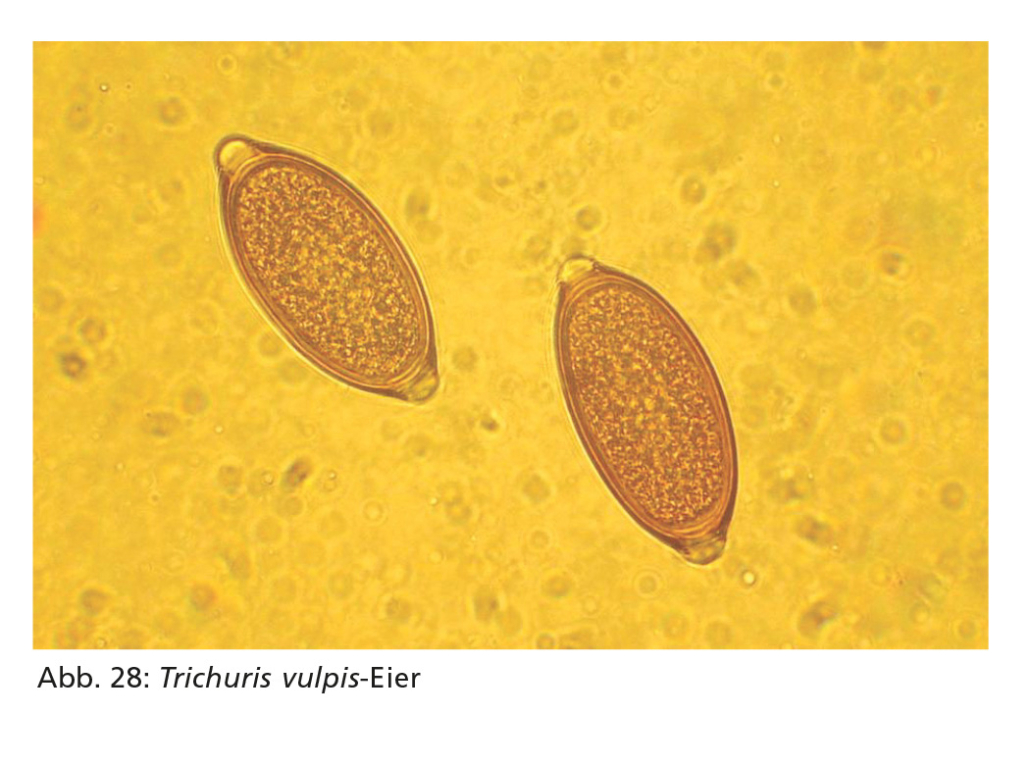
Trichuris-Befall wird im Kot (4–10 g) mittels Flotationsverfahren durch den Nachweis der charakteristischen zitronenförmigen Eier diagnostiziert. Dabei ist auf eine geeignete Flotationslösung zu achten. Seit einiger Zeit ist zudem ein Kopro-Antigen-ELISA zum Nachweis von Trichuris-Antigen verfügbar. Dieser ermöglicht die Detektion einer Peitschenwurminfektion bereits gut drei Wochen nach der Infektion und somit bis zu sechs Wochen vor Ende der Präpatenz.
Gegen T. vulpis können entsprechend zugelassene, nematodizid wirkende Anthelminthika eingesetzt werden. Häufig sind wiederholte Behandlungen (3–5 Tage, entsprechend Packungsbeilage) erforderlich, um eine vollständige Wirkung zu erzielen. Klinische Fälle treten vor allem unter Haltungsbedingungen auf, die eine erhebliche Kontamination der Umgebung mit Eiern und damit Reinfektionen erlauben (z. B. Gruppenhaltung auf Naturboden, Haltung auf Einstreu). Es ist unter praktischen Gesichtspunkten nur schwer möglich, ein einmal mit Eiern kontaminiertes Erdreich zu dekontaminieren; dazu müsste das oberflächliche Erdreich abgetragen und ersetzt werden. Eine Versiegelung der Böden (z. B. durch Betonieren) erleichtert die mechanische Reinigung und anschließende Desinfektion eines Auslaufs.
Weitere Informationen zu den Charakteristika von T. vulpis, Risikofaktoren, klinischen Anzeichen, Diagnose und Behandlung finden Sie in den Tabellen 6B, 7 und 10 sowie in der ESCCAP-Empfehlung Nr. 4 Parasitological Diagnosis in Cats, Dogs and Equines.
5.7. Zwergfadenwürmer (Strongyloides stercoralis)
Strongyloides stercoralis ist ein weltweit vorkommender zoonotischer Nematode von Caniden und Primaten mit im Dünndarm lebenden adulten Würmern (3–8 mm und schlank). Er kommt am häufigsten in tropischen und subtropischen Regionen vor, kann aber auch in gemäßigten Regionen oder in Nordeuropa auftreten. Katzen infizieren sich seltener mit S. stercoralis als Hunde. In ihrem komplexen Lebenszyklus sind nur weibliche Würmer parasitär. Die erwachsenen Weibchen sind in die Darmschleimhaut eingebettet und vermehren sich ungeschlechtlich durch Parthenogenese, wobei sie Eier in das Darmlumen abgeben, die bald schlüpfen können. Daher werden häufig bereits L1 (rhabditiforme Larven) mit dem Kot ausgeschieden. Die mit dem Kot ausgeschiedenen L1 können sich innerhalb von 24 Stunden im Boden zu L3 entwickeln oder zu nicht parasitären weiblichen und männlichen Würmern heranreifen, die sich in der Umgebung sexuell fortpflanzen können. Dieser Prozess kann zu einer massiven Vermehrung und Kontamination der Umgebung führen. Die infektiösen L3 infizieren den Wirt durch perkutane, orale oder laktogene Übertragung. Selten kommt es bei Hunden zu einer Autoinfektion, d. h. L1 entwickeln sich im Darm zu L3 im selben Individuum.
Strongyloides-Infektionen verlaufen oft moderat und subklinisch, und die Krankheit tritt hauptsächlich bei massiv infizierten Neugeborenen und Säuglingen auf. Bei kranken Hunden treten bei schweren Infektionen Lungenentzündungen und wässriger bis schleimiger Durchfall auf. Oftmals sind die Tiere stark abgemagert, und eine verlangsamte Wachstumsrate kann eines der ersten klinischen Anzeichen sein. Der Appetit ist in der Regel gut, und der Hund (oder die Katze) ist in den frühen Phasen der Krankheit normalerweise aktiv. In der Regel stehen Infektionen mit warmen, feuchten, überfüllten und unhygienischen Unterkünften in Zusammenhang.
Die Diagnose von S. stercoralis bei Hunden beruht auf dem Nachweis von L1 im Kot mittels Baermann-Verfahren. Die Proben müssen so frisch wie möglich sein, und die Untersuchung mehrerer Proben erhöht die diagnostische Sensitivität. Larven können nur gelegentlich bei Anwendung des Flotationsverfahrens beobachtet werden. Die Spezifität der Diagnose ergibt sich aus der morphologischen Identifizierung der charakteristischen Merkmale der L1 (z. B. langer rhabditischer Ösophagus und gerader Schwanz), wodurch sie von anderen parasitären oder freilebenden Arten unterschieden werden können. Gelegentlich können Larveneier (50–60 × 30–35 μm) durch Flotation von frischem Kot identifiziert werden. Einige diagnostische Labore bieten einen Kot-PCR-Test an.
Zuchten und der Tierhandel scheinen eine wichtige epidemiologische Rolle bei der Verbreitung von S. stercoralis zu spielen. Da die routinemäßig mittels Flotationsverfahren durchgeführte Kotuntersuchung nur eine geringe Sensitivität für den Nachweis von L1 aufweist und die Ausscheidung von Eiern selten ist, könnte die Prävalenz sowie die klinische Bedeutung von S. stercoralis bei Hunden unterschätzt werden.
Schlechte Hygienebedingungen und die gemeinsame Unterbringung von anfälligen und infizierten Hunden können zu einer raschen Ausbreitung der Infektion bei allen Hunden in einer Tierhaltung führen. Hunde mit Durchfall sollten umgehend von gesund erscheinenden Hunden isoliert werden. Direkte Sonneneinstrahlung, erhöhte Boden- oder Oberflächentemperaturen und Austrocknung sind für alle freien Larvenstadien schädlich. Durch gründliches Waschen von Holz und undurchlässigen Oberflächen mit Dampf oder konzentrierten Salz- oder Kalklösungen, gefolgt von Spülen mit heißem Wasser, wird der Parasit wirksam vernichtet.
In den letzten Jahren haben molekulare und epidemiologische Studien darauf hingedeutet, dass sowohl an Hunde angepasste als auch zoonotische Populationen von S. stercoralis existieren könnten. Da die Krankheit beim Menschen schwerwiegend sein kann, ist beim Umgang mit infizierten Hunden Vorsicht geboten. Die Krankheit verläuft beim Menschen (wie auch beim Hund) viel wahrscheinlicher schwer, wenn der Patient immunsupprimiert ist.
Infektionen bei Hunden können versuchsweise mit Ivermectin (0,2 mg/kg/Tag, oral an zwei aufeinanderfolgenden Tagen, off-label, definitiv nicht empfohlen bei Ivermectin-empfindlichen Hunden) oder Fenbendazol (50 mg/kg/Tag, oral über 5 Tage, 4 Wochen später wiederholen) behandelt werden. In Einzelfällen wurden höhere Dosierungen, zusätzliche Wiederholungen der Behandlungen oder sogar die Kombination von Ivermectin und Fenbendazol eingesetzt, um die Infektionen zu beseitigen. Bei Katzen kann Fenbendazol (50 mg/kg/Tag, oral über 3 Tage) verabreicht werden. Diese Behandlungen sind weder bei Katzen noch bei Hunden zugelassen. Bei allen Tieren sollte der Kot mindestens 6 Monate nach der Behandlung regelmäßig untersucht werden, um die Wirksamkeit zu bestätigen.
6. Diagnose von Wurminfektionen
Patente Infektionen der meisten genannten Helminthen können durch Kotuntersuchungen nachgewiesen werden. Ausnahmen sind D. immitis und D. repens, für deren Diagnose eine Blutprobe auf Mikrofilarien, Antigene oder Antikörper (nur Katze) untersucht wird (Tabelle 10 und 11).
Koproskopische Untersuchungen zum Nachweis von Wurmeiern sollten mit einer Probe von mindestens 4–10 g Kot durchgeführt werden. Um die Nachweissicherheit zu erhöhen, können mehrere Proben, z. B. von drei aufeinanderfolgenden Tagen, einzeln untersucht werden. Proben sollten stets von frisch abgesetztem Kot genommen werden und nicht von bereits länger im Zwinger oder Auslauf liegendem Kot.
Für den Nachweis von Spul-, Haken-, Peitschen- und Gurkenkernbandwurminfektionen sind kommerzielle Kopro-Antigen-ELISAs verfügbar. Geeignete Untersuchungsmethoden sind z. B. die modifizierte McMaster-Methode oder andere Flotationstechniken (Tabelle 6 und 7). Eier von Spulwürmern, Hakenwürmern, Peitschenwürmern und den meisten Bandwürmern sind mikroskopisch leicht zu erkennen. Allerdings ist die Nachweissicherheit von Taeniiden-Infektionen mittels koproskopischer Verfahren sehr gering. Bei Hunden muss darauf geachtet werden, dass durch Koprophagie falsch positive Ergebnisse resultieren können, welche durch wiederholte Untersuchungen oder die Verwendung von Kopro-Antigen Untersuchungen ausgeschlossen werden können.
Zum Nachweis von Nematoden-Larven im Kot (Lungenwurmlarven, S. stercoralis) wird das Trichter-Auswanderverfahren (Baermann-Methode) eingesetzt (Tabelle 10 und 11). Aufgrund variierender Ausscheidung sollte wenn möglich über drei aufeinanderfolgende Tage Kot gesammelt und dieser jeweils unmittelbar untersucht werden. Die Differenzierung basiert auf der Länge der Larven und der Morphologie des Schwanzes. Auch für manche Anthelminthika-Präparate wird ca. drei Wochen nach der Behandlung eine Kotuntersuchung empfohlen, um eine gegebenenfalls notwendige Wiederholungsbehandlung zu prüfen. Alternativ kann ein kommerziell erhältlicher Antigen-Test zum serologischen Nachweis von A. vasorum in klinischen Verdachtsfällen verwendet werden. Klinisch an Angiostrongylose erkrankte Hunde sollten zudem hinsichtlich ihres Lungen- sowie Herzbefunds und ihrer Gerinnungsparameter untersucht werden.
Grundsätzlich sollte unabhängig von eventuellen Entwurmungen mindestens einmal im Jahr eine gründliche diagnostische Untersuchung mit dem Ziel einer Statuserhebung vorgenommen werden.
Eine ausführliche bebilderte Anleitung für die Diagnostik im Rahmen der Bekämpfung von Würmern bei Hunden und Katzen steht zum kostenlosen Download auf www.esccap.de zur Verfügung sowie in der ESCCAP-Empfehlung Nr. 4 Parasitological Diagnosis in Cats, Dogs and Equines.
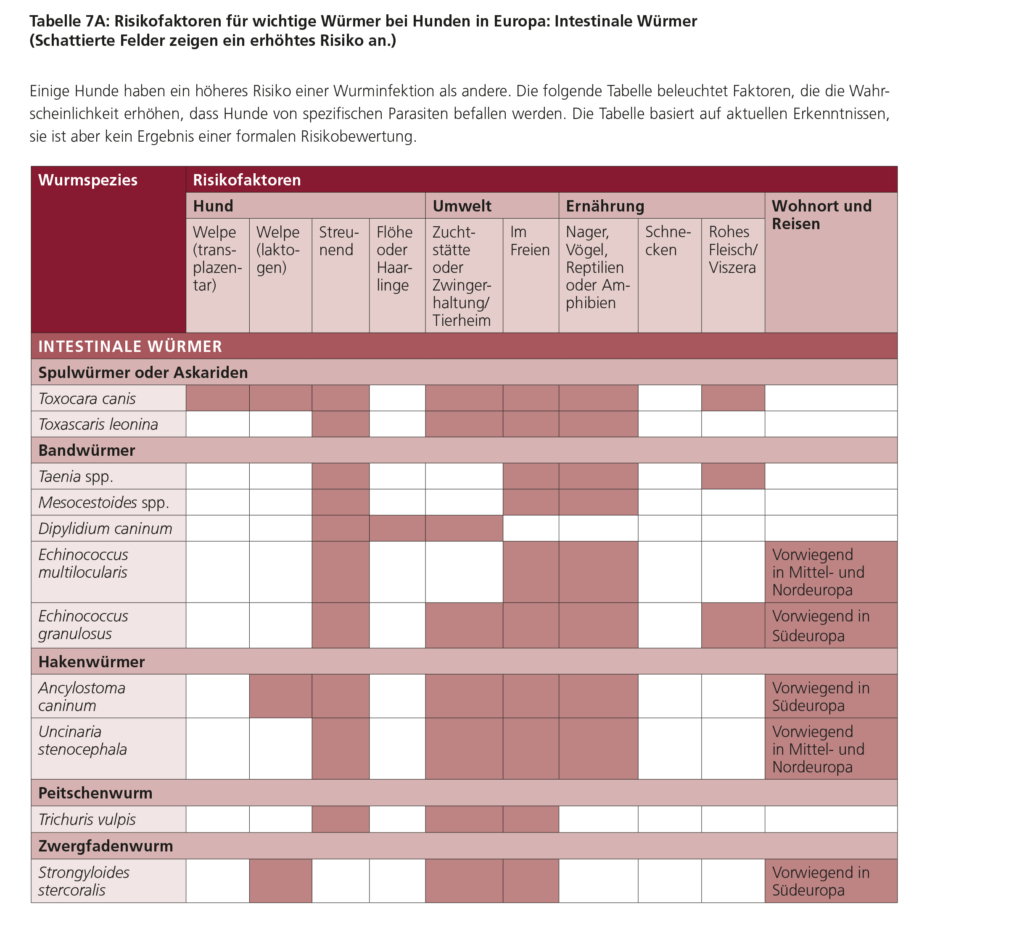
7. Individuelle Faktoren: Alter, Nutzung, Haltung, Ernährung und Reisen
Je nach Alter, Haltungsform, Ernährung und Nutzung von Hund und Katze müssen Diagnostik, Medikation und Prävention individuell vorgenommen werden. Bestimmte Faktoren können ein intensiveres Monitoring und/oder eine frequentere Entwurmung erforderlich machen, während andere ein weniger intensives Vorgehen rechtfertigen können. Bei der Erstellung des Maßnahmenplans sollten unter anderem folgende Aspekte berücksichtigt werden (siehe auch Tabellen 6 und 8):
Alter, Zucht
- Hunde- und Katzenwelpen tragen im Allgemeinen ein höheres Risiko, an parasitären Infektionen zu erkranken und diese zu übertragen, als adulte Tiere.
- Gravide Hündinnen und laktierende Hündinnen können T. canis, letztere zusätzlich noch den in Deutschland sehr selten vorkommenden Hakenwurm A. caninum auf ihre Welpen übertragen und sich darüber hinaus selbst bei den Welpen infizieren (Superinfektion).
- Laktierende Kätzinnen können T. cati auf ihre Welpen übertragen und sich darüber hinaus selbst bei den Welpen infizieren (Superinfektion).
Haltungsform, Nutzung
Folgende Hunde- und Katzengruppen tragen ein höheres Risiko als einzeln im Haus gehaltene Tiere:
- Hunde und Katzen in Zuchten, Zwingern oder Tierheimen bzw. in Haushalten mit mehreren Tieren
- Im Freien lebende Hunde und Katzen sowie solche, die unbeaufsichtigten Auslauf haben
- Jagende Hunde und Katzen
- Hunde (und Katzen) mit der Neigung, alles zu fressen
Ernährung
- Hunde und Katzen mit Zugang zu wilden Nagetieren, Schnecken, rohem Fleisch oder rohem Fisch einschließlich Viszera, Kadavern und nicht ausreichend erhitzten oder gefrorenen Schlachtabfällen haben ein höheres Risiko als andere Tiere.
Wohnort und Reisen
- Tiere, die in endemischen Regionen oder Orten mit hohem Infektionsdruck leben oder diese besuchen (z. B. Urlaub, Tierpensionen, Hunde- und Katzenausstellungen, Leistungsprüfungen etc.), tragen ein erhöhtes Risiko, sich mit den in diesen Regionen endemischen Parasiten zu infizieren.
Auf Basis der spezifischen Voraussetzungen eines Tieres sollten Art und Umfang von Diagnostik, Prävention und Medikation im Rahmen untenstehender Empfehlungen individuell ausgewählt werden. Inwieweit die gewählten Maßnahmen für eine Bekämpfung eines Wurmbefalls ausreichend und geeignet sind, klärt sich über eine Diagnostik, anhand derer der Erfolg der Prävention oder Medikation überprüft werden kann.
Rohfleischfütterung (Barfen)
Über rohes Fleisch und Innereien (z. B. Leber, Lunge) können verschiedene Parasiten auf Hunde und Katzen übertragen werden. Dazu zählen unter anderem der gefährliche Hundebandwurm (Echinococcus granulosus-Gruppe), verschiedene Taenia-Arten, Spulwürmer der Gattung Toxocara, der Erreger der Toxoplasmose (Toxoplasma gondii) und andere einzellige Parasiten wie Sarcocystis spp. und Neospora caninum. Wie hoch das Risiko ist, dass sich Hunde und Katzen über rohes Fleisch mit diesen und anderen Erregern anstecken, ist bisher unbekannt. Sicher ist nur, dass es möglich ist und immer wieder vorkommt. Dies heißt jedoch nicht, dass Hunde und Katzen aus parasitologischer Sicht grundsätzlich nicht roh ernährt werden dürfen. Wichtig ist, dass das Fleisch vor dem Verfüttern ausreichend tief und lange eingefroren wird, um enthaltene Parasitenstadien abzutöten. Empfohlen wird, dass das Fleisch mindestens eine Woche bei -17 °C bis -20 °C tiefgefroren bleibt. Wer nicht weiß, ob das von ihm gekaufte Fleisch diese Voraussetzungen erfüllt, selbst kein entsprechendes Einfrieren gewährleisten kann, aber dennoch roh füttern möchte, der sollte bei seinem Vierbeiner alle vier Wochen eine Kotuntersuchung vornehmen lassen oder ihn mit einem gegen Spulwürmer wirksamen Produkt entwurmen. Aufgrund der sehr niedrigen Nachweissicherheit von Bandwurminfektionen mittels Kotuntersuchungen ist an deren Stelle stets eine Behandlung ratsam. Denn: Auch wenn das Risiko einer Ansteckung über rohes Fleisch nicht besonders hoch ist, können die gesundheitlichen Folgen von Infektionen für Tier und Mensch erheblich sein. Ein Schutz vor über das Barfen übertragbaren Protozoen ist durch die Anwendung von Antiparasitika nicht möglich.
8. Resistenzen gegen Anthelminthika und Bekämpfung von Parasitenstadien in der Umwelt
Resistenzen von Anthelminthika
Grundsätzlich gibt es für Europa keine wissenschaftlich bestätigten Berichte über Anthelminthika-Resistenzen bei Helminthen von Hund oder Katze. Allerdings wurden zuletzt mehrere Berichte zu Anthelminthika-Resistenzen bei Ancylostoma caninum-Populationen sowie in zwei Fällen bei Dipylidium caninum in den USA veröffentlicht. Vereinzelt wurde in der Vergangenheit zudem über vermutete Anthelminthika-Resistenzen bei Toxocara canis in den USA berichtet. Kürzlich wurde allerdings in einem aus Spanien in die Schweiz importierten Hund eine Praziquantel-resistente D. caninum-Population nachgewiesen. Zudem ist seit längerem bekannt, dass bei Dirofilaria immitis Resistenzen gegenüber makrozyklischen Lactonen (ML) in den USA vorkommen, und diesbezüglich gab es vor Kurzem einen Bericht über eine ML-Resistenz bei D. immitis in einem aus den USA nach Europa importierten Hund. Der Umstand, dass für Europa und somit auch Deutschland bisher keinerlei Berichte über ein relevantes Vorkommen von Anthelminthika-Resistenzen bei Würmern von Hund und Katze vorliegen, kann als Hinweis auf eine weiterhin sehr gute Wirksamkeit der verfügbaren Anthelminthika betrachtet werden. Allerdings ist dies lediglich eine nicht durch wissenschaftliche Daten gestützte Vermutung, denn es liegen keine systematischen Untersuchungen auf diesem Gebiet vor.
Auf Basis der Erfahrungen aus der Großtierpraxis, wo Resistenzen nachgewiesenermaßen existieren, ist die Wahrscheinlichkeit von Resistenzentwicklungen in größeren Hunde- und Katzenbeständen wie Tierheimen, großen Zuchten oder ähnlich intensiven Haltungsformen vermutlich erhöht. Denn immer dort, wo eine simultane Behandlung mehrerer Tiere mit demselben Produkt einen hohen Selektionsdruck auf die lokale Parasitenpopulation zur Folge hat, kann die Wahrscheinlichkeit einer Entwicklung von Resistenzen erhöht sein. Dementsprechend traten die o. a. Resistenzen bei Hakenwurmpopulationen in den USA zuerst bei intensiv gehaltenen und hochfrequent entwurmten Windhunden, jedoch inzwischen auch bei anderen Rassen auf.
Es wird daher empfohlen, die Bekämpfung von Würmern in größeren Hunde- und Katzenbeständen wie Tierheimen, großen Zuchten oder ähnlich intensiven Haltungsformen sorgfältig zu planen und durch Untersuchungen von Kotproben zu begleiten. Ziel ist es, vorhandene Wurmspezies zu diagnostizieren und die Wirksamkeit der getroffenen Maßnahmen kontinuierlich zu überprüfen. Zudem sollten durch begleitende Maßnahmen (v. a. Hygiene) die Entwurmungshäufigkeiten auf ein für die Gesundheitsvorsorge angemessenes Maß beschränkt werden.
Bekämpfung von Parasitenstadien in der Umwelt
Die Bekämpfung von Helminthenstadien (Eier, Larven) in der Umwelt und die Reduktion der Ausscheidung von Wurmstadien durch Hunde und Katzen ist wesentlich, um den Infektionsdruck auf Tiere und Menschen (Zoonose) zu minimieren.
Die Kontamination der Umwelt durch Hunde und Katzen findet über eine Ausscheidung von Parasitenstadien mit dem Kot statt.
Eine Rolle bei der Kontamination der Umwelt spielen auch Füchse, die sehr häufig mit „Hundeparasiten” befallen sind, und zwar sowohl in ländlichen als auch in urban geprägten Regionen. Darüber hinaus stellen freilaufende und verwilderte Katzen ein Reservoir für die Kontamination der Umwelt dar.
Die Infektion von Zwischenwirten oder paratenischen Wirten (z. B. Nagetiere, Vögel und Schnecken) kann zu einer verlängerten Persistenz von Parasitenstadien in der Umgebung der Hunde oder Katzen führen.
Die in der Umwelt befindlichen Stadien von Parasiten überleben teilweise mehrere Monate bis Jahre. Frisch ausgeschiedene Stadien können direkt infektiös sein (z. B. Eier von Taenia, Hydatigera und Echinococcus spp.), andere müssen dagegen bei geeigneten Temperaturen (üblicherweise > 16 °C) über einen Zeitraum von wenigen Tagen bis zu mehreren Wochen eine Entwicklung durchlaufen (z. B. Eier von Nematoden). Wichtigste Voraussetzung zum Schutz vor einer Kontamination der Umwelt sind stringente, umfassende und durchdachte Maßnahmen, die ein Ausscheiden von Parasitenstadien durch Hund und Katze minimieren.
- Zur Minimierung infektiöser Wurmstadien in der Umwelt wird eine regelmäßige Beseitigung und Entsorgung von Hunde- und Katzenkot unbedingt empfohlen. Der Kot sollte täglich entfernt werden und nicht die Toilette hinuntergespült oder auf den Kompost gegeben, sondern über den Hausmüll entsorgt werden. Da es nahezu unmöglich ist, den Kot freilaufender Katzen aufzusammeln, ist die gezielte Entwurmung solcher Tiere eine geeignete Maßnahme, um das Ausscheiden infektiöser Wurmstadien zu minimieren.
- Praktische Unterstützungen für die Beseitigung von Hundekot in der Umgebung wie in Parks und auf Hundeauslaufflächen, etwa das Aufstellen spezieller Abfallbehälter mit Entsorgungstüten, sollten gefördert werden.
- Neben der Entfernung von Kot sind z. B. die Betreuung und Entwurmung streunender Hunde und verwilderter Katzen (z. B. in Zusammenarbeit mit Tierschutzorganisationen) umsichtige und sinnvolle Maßnahmen.
- Kinderspielplätze sollten eingezäunt werden, um Hunde und Katzen (durch sehr hohe, oben abgewinkelte, engmaschige Zäune) fernzuhalten. Ein Hundeverbot in solchen Arealen ist üblich und sollte strikt eingehalten werden. Sandkästen sollten zwischen dem Gebrauch abgedeckt und der Sand regelmäßig ausgetauscht werden (1–2 x im Jahr).
- Da die Eier von Cestoden und Nematoden gegenüber Umwelteinflüssen sehr widerstandsfähig sind und ein Teil davon im Boden über Monate bis Jahre persistieren kann, ist eine Dekontamination nicht ohne sehr aufwendige Maßnahmen zu erreichen und in der Fläche nicht vorstellbar. In Tierheimen oder Zwingern und Zuchten kann dies in bestimmten Fällen die Beseitigung von Sand oder Boden und/oder das Abdecken und Versiegeln von kontaminiertem Boden mit Beton oder Asphalt erforderlich machen. Glatte, versiegelte Oberflächen erleichtern im Allgemeinen die Reinigung und Desinfektion und sind daher insbesondere in Tierheimen und Hundezuchten von Vorteil.
- Da Trockenheit und ultraviolettes Licht Wurmeier schädigen, können direkte Sonneneinstrahlung und Trockenlegung ebenfalls einen Beitrag zur Dekontaminierung leisten.
- Um einer hochgradigen Kontamination von Zuchten, Zwingern oder Tierheimen vorzubeugen, sind strenge Behandlungs- und Quarantänemaßnahmen für Neuankömmlinge unerlässlich.
9. Prävention zoonotischer Parasitosen
Da manche Würmer von Hunden und Katzen für den Menschen infektiös sind, tragen TierärztInnen und TierhalterInnen im Rahmen der Bekämpfung von Endoparasiten beim Tier gleichzeitig Verantwortung für die Gesundheit des Menschen. Ein besonderes Zoonoserisiko besteht bei den weit verbreiteten Spulwürmern der Gattung Toxocara, da es hier nach oraler Aufnahme infektiöser Spulwurmeier durch den Menschen zu einer somatischen Wanderung von Larven kommen kann (Larva migrans visceralis). Die Infektion betrifft hierzulande vor allem Kleinkinder und führt zu meist milden Verläufen, etwa mit leichtem Fieber und Oberbauchschmerzen, wird aber in der Regel gar nicht als solche erkannt. Werden bei dieser somatischen Wanderung Auge, Nervenbahnen und/oder Gehirn des Menschen befallen, kann dies jedoch ernsthafte gesundheitliche Folgen haben.
Infolge einer Infektion mit Echinococcus multilocularis oder der Echinococcus granulosus-Gruppe kommt es beim Menschen zu einer alveolären bzw. zystischen Echinococcose mit Zystenbildung in der Leber und/oder anderen Organen, was besonders im Fall einer E. multilocularis-Infektion sogar tödliche Folgen haben kann. Die Infektion des Menschen findet über die orale Aufnahme von Wurmeiern statt. Hauptquelle für die Kontamination der Umgebung mit Wurmeiern von E. multilocularis ist der Fuchs, möglich ist aber auch ein Infektionsweg mit Wurmeiern, die infizierte Hunde im Fell tragen oder mit dem Kot ausscheiden. Menschen mit Kontakt zu Hunden und Katzen sollten über die Gefahren dieser Zoonosen aufgeklärt werden und wissen, dass bei bestimmten Personen erhöhte Infektionsrisiken bestehen, z. B. bei Personen mit spezifischer verhaltensbedingter (z. B. Säuglinge, Kleinkinder, beeinträchtigte Menschen) oder berufsbedingter (z. B. tiermedizinische Fachangestellte, TierpflegerInnen, FörsterInnen) Exposition.
Wichtige präventive Maßnahmen zum Schutz vor Zoonosen sind:
- Persönliche Hygiene (z. B. Händewaschen, Gartenarbeit mit Handschuhen)
- Kein Verzehr von ungewaschenem rohem Gemüse, Früchten oder Pilzen
- Tierärztlich verordnete Maßnahmen wie regelmäßige anthelminthische Behandlungen von Hund und Katze und/oder regelmäßige parasitologische Untersuchungen
- Konsequentes unschädliches Beseitigen von Hunde- und Katzenkot sowie unter Umständen weitere Maßnahmen gegen eine Umweltkontamination mit Wurmstadien
- Vermeiden einer Exposition, insbesondere von Kindern, gegenüber mit Wurmstadien kontaminierten Umgebungen (z. B. Meidung von Hundewiesen, kotkontaminierten Gärten oder Spielplätzen bzw. Sandkästen)
Informationen zu Zoonosen und geeigneten Maßnahmen zur Prävention sollten für TierhalterInnen in der tierärztlichen Praxis leicht zugänglich gemacht werden.
10. Schulung von Praxisteams, TierbesitzerInnen und der Öffentlichkeit
Empfehlungen und Informationen zur Bekämpfung von Würmern sollten verständlich und einheitlich kommuniziert und umgesetzt werden. Mithilfe von Informationsmaterialien und über verschiedene Medien sollte nicht nur bei Personen, die im (tier-)medizinischen Bereich tätig sind, sondern auch bei TierhalterInnen und der Allgemeinheit Aufmerksamkeit geweckt und die Sensibilität für parasitäre Infektionen sowie das Risiko für Zoonosen, einschließlich klinischer Manifestationen beim Menschen, insbesondere bei Kindern, gefördert werden. Eine enge Zusammenarbeit zwischen Verbänden, TierärztInnen und ÄrztInnen sollte initiiert und gefördert werden, die Vorteile einer solchen Zusammenarbeit bei der Bekämpfung von Zoonosen gilt es, herauszustellen.
TierhalterInnen sollten über potenzielle Gesundheitsrisiken durch Parasiten informiert werden, ohne dass diese dramatisiert werden. Wege zur Vermeidung möglicher Risiken müssen aufgezeigt und konsequent umgesetzt werden. Dies gilt nicht nur für die Risiken, denen die eigenen Tiere ausgesetzt sind, sondern auch für die von Familienmitgliedern und anderen Menschen, die innerhalb des Aktionsradius dieser Tiere leben. Seriöse Informationsmaterialien und Internetseiten sind dabei wertvolle Hilfsmittel. Der Nutzen sinnvoll geplanter Entwurmungen und die Notwendigkeit von „Gesundheits- Checks für Kleintiere“ sollten der allgemeinen Öffentlichkeit bekannt gemacht und in Erinnerung gerufen werden (z. B. durch eindeutige farbige Plaketten [„TÜV“-Plaketten] für jedes Kalenderjahr). Eine verantwortungsvolle Hunde- und Katzenhaltung kann in entscheidendem Maße dazu beitragen, die Akzeptanz von Hunden und Katzen als Begleitern des Menschen nachhaltig zu fördern.
Zusätzliche Informationen und Quellenmaterial stehen zur Verfügung auf der Website: https://www.esccap.de
Stand: Dezember 2025